Ácidu láctico
| Ácidu láctico | |
|---|---|
 | |
| Xeneral | |
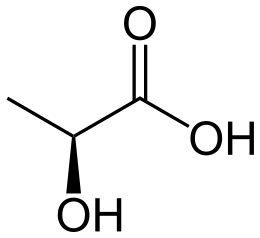
| Estructura química |
 |
| Fórmula química | C₃H₆O₃ |
| SMILES canónicu | modelu 2D |
| MolView | modelu 3D |
| Propiedaes físiques | |
| Masa | 90,031694 unidá de masa atómica |
| Propiedaes termoquímiques | |
| Peligrosidá | |
| Identificadores | |
El ácidu láctico, o la so forma ionizada, el lactato (del lat. lac, lactis, lleche), tamién conocíu pola so nomenclatura oficial ácidu 2-hidroxi-propanoico o acedu α-hidroxi-propanoico, ye un compuestu químicu que desempeña importantes roles en dellos procesos bioquímicos, como la fermentadura láctica. Ye un acedu carboxílico, con un grupu hidroxilo nel carbonu axacente al grupu carboxilo, lo que lo convierte nun acedu α-hidroxílico (AHA) de fórmula H3C-CH(OH)-COOH (C3H6O3). En solución puede perder l'hidróxenu xuníu al grupu carboxilo y convertise nel anión lactato.
L'ácidu láctico ye quiral, polo que pueden atopase dos enantiómeros (isómeros ópticos). Unu ye'l dextrógiro acedu D-(+)-láctico o d-acedu láctico (nesti casu, l'ácidu (R)-láctico); l'otru ye'l levógiro acedu L-(-)-láctico o ℓ-ácidu láctico (nesti casu, acedu (S)-láctico), que ye'l que tien importancia biolóxica. L'amiestu racémica (cantidaes idéntiques d'estos isómeros) llámase d,ℓ-acedu láctico.
Historia[editar | editar la fonte]
Foi refináu per primer vegada pol químicu suecu Carl Wilhelm Scheele en 1780 a partir de lleche agrio. En 1808, Jöns Jacob Berzelius afayó que se lliberar acedu láctico nos músculos al realizar esfuercios físicos intensos.[1] La so estructura foi determinada por Johannes Wislicenus en 1873.
En 1856 Louis Pasteur afayó'l lactobacillus y el so rol na producción d'ácidu láctico. Esti ácidu empezó a ser producíu comercialmente pola compañía alemana Boehringer Ingelheim en 1895.
En 2006 la producción global d'ácidu láctico algamó 275,000 tonelaes con una crecedera permediu añal de 10%.[2]
Importancia biolóxica[editar | editar la fonte]
El ácidu ℓ-láctico producir a partir del acedu pirúvico al traviés de la enzima lactato deshidrogenasa (LDH) en procesos de fermentadura. El lactato produzse de cutio nel metabolismu y sobremanera mientres l'exerciciu, pero nun aumentar la so concentración hasta que l'índiz de producción nun supera al d'eliminación. Este depende de dellos factores, como los tresportadores monocarboxilatos, concentración de LDH y capacidá oxidativa nos texíos. La concentración de lactatos nel sangre usualmente ye de 1 o 2 mmol/l en reposu, pero puede aumentar hasta 20 mmol/l mientres un esfuerciu intensu. Tien de considerase que, a pH fisiolóxicu nel cuerpu humanu, ye dicir 7.35, atópase solo na so forma disociada, esto ye, como lactato y non como acedu.
L'aumentu de la concentración de lactatos asocede xeneralmente cuando la demanda d'enerxía en texíos (principalmente musculares) devasa la disponibilidad d'osíxenu en sangre. So estes condiciones la piruvato deshidrogenasa nun algamar a convertir el piruvato a Acetil-CoA lo suficientemente rápido y el piruvato empieza a atropase. Esto xeneralmente tornaría la glucólisis y amenorgaría la producción d'Adenosín trifosfato (el ATP sirve p'atropar enerxía), si nun fuera porque la lactato deshidrogenasa amenorga'l piruvato a lactato:
piruvato + NAD + H+ → lactato + NAD+
La función de la producción de lactato ye aferruñar NADH + H pa refaer la nicotinamida adenina dinucleótido (NAD+) necesaria pa la glucólisis, y por tanto por que siga la producción de ATP.
El lactato producíu sale de la célula muscular y circula pola riega sanguineu hasta'l fégadu, ónde se vuelve a tresformar en glucosa por gluconeogénesis. Al ciclu qu'entiende la glicólisis na célula muscular y la so reciclaje por gluconeogénesis nel fégadu conózse-y como ciclu de Cori.
El fégadu y el corazón tienen la facultá d'aferruñar el lactato del sangre convirtiéndolo de nuevu a piruvato.
La fermentadura d'ácidu láctico tamién la producen les bacteries Lactobacillus. Estes bacteries pueden atopase na boca, y pueden ser les responsables del progresu de la caries primeramente empecipiada por otres bacteries.
En medicina[editar | editar la fonte]
En condiciones normales, el valor de referencia pal lactato en sangre ye inferior a 2 mmol/L. Mientres l'exerciciu, la concentración de lactato puede amontase dende un nivel mediu de 0.9 mmol/L hasta 12 mmol/L; mientres la hipoxia tisular auméntase la producción d'este y ye un marcador de gravedá. (Rev Med Inst Mex Seguro Soc. 2015;53(3):316-21).
En medicina ye unu de los compuestos de la solución láctica de Ringer, que ye una solución que s'inyecta intravenosamente a les persones cuando sufrieron una perda de sangre por causa de un traumatismu, ciruxía o quemadura.
La solución ta compuesta por 129 mmol/L de Na, 109 mmol/L de cloru y 28 mmol/L de L-lactato. Ye una solución que s'usa alternativamente a la salina fisiolóxica (0.9%) pa recuperar volume. La diferencia d'iones fuertes fai que'l hartman (solución láctica de Ringer) sía utilizáu por dalgunos como terapia na hipovolemia. Sicasí, por tener menos tonicidá (osmolaridad) que la solución salina, dalgunos prefieren esta. L'efectu sobre l'equilibriu acedu-base de la salina va ser promover acidosis (pol cloru), mientres l'efectu del hartman va ser más alcalinizante pola diferencia d'iones fuertes y pol ácidu láctico.
Exerciciu y lactato: esplicación de la acidosis[editar | editar la fonte]
Esti artículu o seición necesita referencies qu'apaezan nuna publicación acreitada, como revistes especializaes, monografíes, prensa diaria o páxines d'Internet fiables. |
Mientres un exerciciu d'intensidá creciente col tiempu, cuando hai demasiada demanda d'enerxía, el lactato produzse más rápido que la capacidá de los texíos pa esanicialo, y entós la concentración de lactato muscular empieza a aumentar. Ye un procesu benéficu, porque la rexeneración de NAD+ asegura que la producción d'enerxía siga y asina tamién l'exerciciu.
Contra lo que se creyó por enforma tiempu, la medría de la cantidá de lactato nun ye causante direutu de l'acidosis nin ye responsable tampoco de les aguyetes (microroturas fibrilares causaes pol exerciciu) o calambres (polo xeneral debíu al sobreesfuerzo). Esto debe en primer llugar a que l'ácidu láctico nun puede lliberar el catión hidróxenu, y en segundu llugar a que'l lactato nun s'atopa como acedu láctico, sinón na so forma base, como lactato. Los analises realizaos na ruta glucolítica indiquen que nun hai abondes cationes hidróxenu presentes como pa formar acedu láctico o cualesquier otru tipu d'ácidu. Ye importante señalar que, a pH fisiolóxicu y a nivel de la célula muscular (miocito) y según el pKa acedu del ácidu láctico (pKa:3.86), lo que s'atopa ye la base, el lactato, y non l'ácidu láctico, por cuenta de que va tar totalmente disociado nestes condiciones.
L'acidosis que munches vegaes acomuñar a la producción de lactato mientres exercicios estremos provién d'una reacción dafechu distinta y separada.[3]
Cuando'l ATP s'hidroliza (esto ye, se "dixebra", n'agua), llibérase un catión hidróxenu, que ye'l principal responsable del amenorgamientu del pH. Mientres exercicios intensos, el metabolismu oxidativo (aerobiosis) nun produz ATP tan rápido como lo demanda'l músculu. Como resultancia, la glucólisis tresformar nel principal productor d'enerxía y puede producir ATP a altes velocidaes. Por cuenta de la gran cantidá de ATP producíu y hidrolizado en tan pocu tiempu, los sistemes amortiguadores de los texíos vense escosos, lo que xenera una cayida del pH y produz acidosis. Ésti ye unu de los factores, ente tantos, que contribúin al dolor muscular agudu esperimentáu pocu dempués del exerciciu intensu.[ensin referencies]
Llogru[editar | editar la fonte]
Fermentadura láctica[editar | editar la fonte]
- A partir del azucre de la lleche (lactosa) con Lactobacillus
- A partir d'almidón, azucre d'uva (glucosa) o azucre de caña (sacarosa) utilizando'l Lactobacillus delbrueckii
El llogru d'acedu láctico con enzimes o microorganismos vivos pueden producir isómeros dextrógiro o levógiros, dependiendo de la enzima arreyada nel procesu.
Síntesis en llaboratoriu[editar | editar la fonte]
Puede llograse un amiestu racémica a partir de etanol, cianuru de sodiu y ácidu sulfúrico:
El procesu termina con un ataque nucleofílico del cianuru al grupu carbonilo del aldehído formando'l nitrilo del ácidu láctico de forma racémica. El nitrilo ye saponificado en presencia d'agua y un escesu d'ácidu sulfúrico pa dar l'ácidu llibre.
Escurrimientu[editar | editar la fonte]
Atopar nel zusmiu de la carne, na lleche aceda, nos músculos y en dellos órganos de delles plantes o animales. Suel mentase como orixe de les aguyetes, el dolor muscular provocáu pol exerciciu repentín ensin tener costume o previu calentamientu. (ver importancia biolóxica).
Aplicaciones y usos[editar | editar la fonte]
Cosmética[editar | editar la fonte]
Utilízase como l'alternativa más amplia al usu de la glicerina como suavizante. Ye usáu principalmente como químicu anti-edá p'anidiar contornes; amenorgar el dañu producíu pola lluz solar; p'ameyorar la testura y el tonu de la piel, y l'aspeutu polo xeneral.
Sicasí tienen de tomase serios procuros al utilizar cosméticos con acedu láctico, porque aumenten la sensibilidá a los rayos ultravioleta del sol.
Alimentos[editar | editar la fonte]
L'ácidu láctico ye utilizáu en dellos productos como regulador d'acidez. Anque puede llograse de la lactosa (azucre de la lleche), la mayor parte del ácidu láctico emplegáu comercialmente deriva del usu de bacteries como la Bacillus acidilacti, Lactobacillus delbrueckii o Lactobacillus bulgaricus pa lleldar fontes de carbohidratos como la maicena y les pataques. Asina, lo que comúnmente se denomina "lleche acedo" n'alimentos vexetarianos o veganos tienen acedu láctico como ingrediente.
Otres aplicaciones[editar | editar la fonte]
- Alimento pa neños.
- Purgante, na forma de lactato de calciu o lactato de magnesiu.
- Aditivu n'alimentos o arumes, na forma de lactato de etilo.
- Removedor de sales de calciu.
- Como mordiente.
- Curtimiento de pieles.
- Materia primo pa síntesis orgánica.
- Aición acaricida: Ye utilizáu nel control del varroasis, ácaru qu'ataca l'abeya melífera Apis mellifera.
- Materia primo pa Biopolímeros.
Referencies[editar | editar la fonte]
- ↑ Roth, Stephen M. (23 de xineru de 2006). «Why does lactic acid build up in muscles? And why does it cause soreness?» (inglés). Scientific American. Consultáu'l 11 de xineru de 2015.
- ↑ «NNFCC Renewable Chemicals Factsheet: Lactic Acid» (inglés). NNFCC (3 de febreru de 2010). Consultáu'l 11 de xineru de 2015.
- ↑ Fisioloxía de la acidosis nel exerciciu estremu
Enllaces esternos[editar | editar la fonte]
Error de Lua en Módulu:Control_d'autoridaes na llinia 522: attempt to index field 'datavalue' (a nil value).


