Ácidu carboxílico

Los ácidos carboxílicos constitúin un grupu de compuestos, carauterizaos porque tienen un grupu funcional llamáu grupu carboxilo o grupu carboxi (–COOH). Nel grupu funcional carboxilo coinciden sobre'l mesmu carbonu un grupu hidroxilo (-OH) y carbonilo (-C=O). Puede representase como -COOH o -CO2H.
Carauterístiques y propiedaes[editar | editar la fonte]
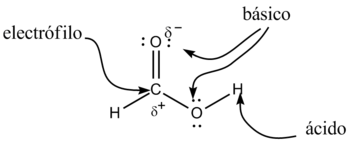
Los ácidos carboxílicos tienen como fórmula xeneral R-COOH. Tienen propiedaes acedes; los dos átomos d'osíxenu son electronegativos y tienden a atraer a los electrones del átomu d'hidróxenu del grupu hidroxilo colo que se debilita l'enllaz, produciéndose en ciertes condiciones una rotura heterolítica, dexando'l correspondiente protón o hidrón, H+, y quedando el restu de la molécula con carga -1 debíu al electrón que perdió l'átomu d'hidróxenu, polo que la molécula queda como R-COO-.
Amás, nesti anión, la carga negativa distribúyese (se deslocaliza) simétricamente ente los dos átomos d'osíxenu, de forma que los enllaces carbonu-osíxenu adquieren un calter d'enllaz parcialmente doble.
Estos non solo son importantes y esenciales pola so propia naturaleza, sinón qu'amás son la materia primu al momentu de preparar los derivaos de acilo, tales como : los cloruros d'ácidu, los ésteres,les amidas, y los tioésteres. Ensin cuntar que na mayoría de les rutes biolóxiques tán presentes.
Xeneralmente los ácidos carboxílicos son ácidos débiles, con namái un 1 % de les sos molécules disociadas pa dar los correspondientes iones, a temperatura ambiente y en disolución aguacienta.
Pero sí son más acedos qu'otros, nos que nun se produz esa deslocalización electrónica, como por casu los alcoholes. Esto debe a que la estabilización por resonancia o deslocalización electrónica, provoca que la base conxugada del ácidu sía más estable que la base conxugada del alcohol y poro, la concentración de protones provenientes de la disociación del ácidu carboxílico sía mayor a la concentración d'aquellos protones provenientes del alcohol; fechu que se verifica esperimentalmente polos sos valor relativos menores de pKa. El ion resultante, R-COO-, nomar col sufixu "-arreyo".

Por casu, el anión procedente del acedu acético llámase ion acetato. Al grupu RCOO- denominar carboxilato.

Síntesis[editar | editar la fonte]
Víes industriales[editar | editar la fonte]
Les síntesis industriales de los ácidos carboxílicos difieren xeneralmente de les usaes a pequeña escala (nel llaboratoriu) porque riquen equipamientu especializáu.
- Oxidación d'aldehídos con aire, utilizando catalizadores de cobaltu y manganesu. Los aldehídos necesarios son llograos fácilmente a partir d'alquenos por hidroformilación.
- Oxidación d'hidrocarburos usando aire. Pa los alcanos más simples, el métodu nun ye selectivu. Los compuestos alílicos y bencílicos sufren oxidaciones más selectives. Los grupos arriendo nun aniellu bencénico aferruñar hasta'l grupu carboxilo (-COOH), ensin importar el llargor previu de la cadena. La formación d'acedu benzoico a partir del tolueno, d'acedu tereftálico a partir del p-xileno, y d'acedu ftálico a partir del o-xileno, son delles conversiones ilustratives a gran escala. El ácidu acrílico xenerar a partir del propeno.[1]
- Deshidrogenación d'alcoholes, catalizada por bases.
- La carbonilación ye'l métodu más versátil cuando va acompañáu a la adición d'agua. Esti métodu ye efectivu pa alquenos que xeneren carbocationes secundarios y terciarios, por casu, d'isobutileno a acedu piválico. Na reacción de Koch, la adición d'agua y monóxidu de carbonu (CO) a alquenos ta catalizada por acedos fuertes. El acedu acético y el ácidu fórmico son producíos pola carbonilación del metanol, llevada a cabu con yodu y alcóxido, quien actúen como promotores, y frecuentemente con altes presiones de monóxidu de carbonu, xeneralmente arreyando dellos pasos hidrolíticos adicionales, nel procesu Monsanto y el procesu Cativa. Les hidrocarboxilaciones arreyen la adición simultánea d'agua y CO. Tales reacciones son llamaes delles vegaes como "Química de Reppe":
- HCCH + CO + H2O → CH2=CHCO2H
- Dellos acedos carboxílicos de cadena llarga son llograos pola hidrólisis de los triglicéridos llograos d'aceites y grases de plantes y animales. Estos métodos tán rellacionaos cola ellaboración del xabón.
Métodos de llaboratoriu[editar | editar la fonte]
Los métodos de preparación pa reacciones a pequeña escala con fines d'investigación, instrucción, o producción de pequeñes cantidaes de productos químicos suelen utilizar reactivos caros.
- Oxidación d'alcoholes primarios con axentes oxidantes fuertes como'l dicromato de potasiu, el reactivu de Jones, el permanganato de potasiu, o'l clorito de sodiu. El métodu ye afechu en condiciones de llaboratoriu, comparáu col usu industrial del aire, pero esti postreru ye más ecolóxicu, yá que conduz a menos subproductos inorgánicos, tales como óxidos de cromu o manganesu.
- Rotura oxidativa d'olefines, por ozonólisis, permanganato de potasiu, o dicromato de potasiu.
- Los ácidos carboxílicos tamién pueden llograse pola hidrólisis de los nitrilos, ésteres, o amides, xeneralmente con catálisis aceda o básica.
- Carbonilación d'un reactivu d'organolitio o Grignard:
- RLi + CO2 → RCO2Li
- RCO2Li + HCl → RCO2H + LiCl
- Halogenación de metilcetonas, siguida d'hidrólisis na reacción del haloformo
- La reacción de Kolbe-Schmitt, qu'aprove una ruta de síntesis al acedu salicílico, precursor de l'aspirina
Reacciones menos comunes[editar | editar la fonte]
Munches reacciones conducen a acedos carboxílicos, pero son usaes namái en casos bien específicos, o principalmente son d'interés académicu:
- Dismutación d'un aldehído na reacción de Cannizzaro.
- Transposición de dicetonas, na Transposición del ácidu bencílico, arreyando la xeneración d'acedos benzoicos na reacción de von Richter, a partir de nitrobencenos, y na reacción de Kolbe-Schmitt, a partir de fenoles.
Reacciones[editar | editar la fonte]
- Llogru de sales d'acedos carboxílicos y amidas a partir del ácidu:
- Los ácidos carboxílicos reaccionen con bases pa formar sales. Nestos sales l'hidróxenu del grupu -OH reemplázase col ion d'un metal, por casu Na+. D'esta forma, l'ácidu acético reacciona con hidrogenocarbonato de sodiu pa dar acetato de sodiu, dióxidu de carbonu y agua.
Entós, depués de llograr el sal, podemos calecer la mesma pa llegar a la amida por aciu deshidratación.[2] La reacción xeneral y el so mecanismu son los siguientes:
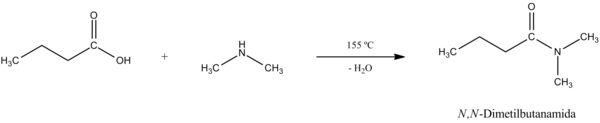


- Formación de derivaos de deshidratación, como anhídridos y cetenes.
- Halogenación na posición alfa: Llamada Halogenación de Hell-Volhard-Zelinsky o tamién conocida como Reacción de Hell-Volhard-Zelinsky. La mesma sustitúi un átomu d'hidróxenu na posición alfa con un halóxenu, reacción que presenta utilidá sintética por cuenta de la introducción de bonos grupos salientes na posición alfa.

Los grupos carboxilos reaccionen colos grupos amino pa formar amides. Nel casu d'aminoácidos que reaccionen con otros aminoácidos pa dar proteínes, al enllaz de tipu amida que se forma denominar enllaz peptídico. Igualmente, los ácidos carboxílicos pueden reaccionar con alcoholes pa dar ésteres, o bien con halogenuros pa dar halogenuros d'ácidu, o ente sigo pa dar anhídridos. Los ésteres, anhídridus, halogenuros d'ácidu y amidas llámense derivaos d'ácidu.
- La Reacción de Varrentrapp tien poques aplicaciones en resume, pero ye útil na determinación de ciertos ácidos grasos. Consiste na descomposición d'acedos grasos insaturados n'otros de cadena más curtia con desprendimientu d'hidróxenu.
- Na Reacción de Arndt-Eistert inxertar un metileno α a un ácidu carboxílico.
Nomenclatura[editar | editar la fonte]
Los ácidos carboxílicos nomar cola ayuda de la terminación –oico o –ico que se xune al nome del hidrocarburu de referencia y anteponiendo la pallabra acedu:
Exemplu
CH3-CH2-CH3 propanu CH3-CH2-COOH
Acedu propanoico (propan + oico)
Los nomes triviales de los ácidos carboxílicos designar según la fonte natural de la que primeramente s'aisllaron. Clasificáronse asina:
| Nome trivial | Nome IUPAC | Estructura |
|---|---|---|
| Ácidu fórmico | Acedu metanoico | HCOOH |
| Acedu acético | Acedu etanoico | CH3COOH |
| Acedu propiónico | Acedu propanoico | CH3CH2COOH |
| Acedu butírico | Acedu butanoico | CH3(CH2)2COOH |
| Acedu valérico | Acedu pentanoico | CH3(CH2)3COOH |
| Acedu caproico | Acedu hexanoico | CH3(CH2)4COOH |
| Acedu enántico | Acedu heptanoico | CH3(CH2)5COOH |
| Acedu caprílico | Acedu octanoico | CH3(CH2)6COOH |
| Acedu pelargónico | Acedu nonanoico | CH3(CH2)7COOH |
| Acedu cáprico | Acedu decanoico | CH3(CH2)8COOH |
| - | Acedu undecanoico | CH3(CH2)9COOH |
| Acedu láurico | Acedu dodecanoico | CH3(CH2)10COOH |
| - | Acedu tridecanoico | CH3(CH2)11COOH |
| Acedu mirístico | Acedu tetradecanoico | CH3(CH2)12COOH |
| - | Acedu pentadecanoico | CH3(CH2)13COOH |
| Acedu palmítico | Acedu hexadecanoico | CH3(CH2)14COOH |
| Acedu margárico | Acedu heptadecanoico | CH3(CH2)15COOH |
| Acedu esteárico | Acedu octadecanoico | CH3(CH2)16COOH |
| - | Acedu nonadecanoico | CH3(CH2)17COOH |
| Acedu araquídico | Acedu eicosanoico | CH3(CH2)18COOH |
| - | Acedu heneicosanoico | CH3(CH2)19COOH |
| Acedu behénico | Acedu docosanoico | CH3(CH2)20COOH |
| - | Acedu tricosanoico | CH3(CH2)21COOH |
| Acedu lignocérico | Acedu tetracosanoico | CH3(CH2)22COOH |
| Acedu pentacosanoico | CH3(CH2)23COOH | |
| Acedu cerótico | Acedu hexacosanoico | CH3(CH2)24COOH |
| - | Acedu heptacosanoico | CH3(CH2)25COOH |
| Acedu montánico | Acedu octacosanoico | CH3(CH2)26COOH |
| - | Acedu nonacosanoico | CH3(CH2)27COOH |
| Acedu melísico | Acedu triacontanoico | CH3(CH2)28COOH |
| - | Acedu henatriacontanoico | CH3(CH2)29COOH |
| Acedu laceroico | Acedu dotriacontanoico | CH3(CH2)30COOH |
| Acedu psílico | Acedu tritriacontanoico | CH3(CH2)31COOH |
| Acedu gédico | Acedu tetratriacontanoico | CH3(CH2)32COOH |
| Acedu ceroplástico | Acedu pentatriacontanoico | CH3(CH2)33COOH |
| - | Acedu hexatriacontanoico | CH3(CH2)34COOH |
| Nome común | Nome IUPAC | Fórmula química | Fórmula estructural |
|---|---|---|---|
| Acedu oxálico | acedu etanodioico | HOOC-COOH | |
| Acedu malónico | acedu propanodioico | HOOC-(CH2)-COOH | |
| Acedu succínico | acedu butanodioico | HOOC-(CH2)2-COOH | 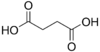
|
| Acedu glutárico | acedu pentanodioico | HOOC-(CH2)3-COOH | |
| Acedu adípico | Acedu hexanodioico | HOOC-(CH2)4-COOH | 
|
| Acedu pimélico | acedu heptanodioico | HOOC-(CH2)5-COOH | |
| Acedu subérico | acedu octanodioico | HOOC-(CH2)6-COOH | 
|
| Acedu azelaico | acedu nonadioico | HOOC-(CH2)7-COOH | |
| Acedu sebácico | acedu decadioico | HOOC-(CH2)8-COOH | 
|
| Acedu maleico | Acedu cis-butenodioico | HOOC-CH=CH-COOH | 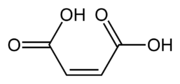
|
| Acedu fumárico | Acedu trans-butenodioico | HOOC-CH=CH-COOH | 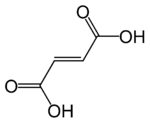
|
| Acedu ftálico | ácidu beceno-1,2-dicarboxílico o-acedu ftálico |
C6H4(COOH)2 | 
|
| Acedu isoftálico | ácidu beceno-1,3-dicarboxílico m-acedu ftálico |
C6H4(COOH)2 | 
|
| Acedu tereftálico | ácidu beceno-1,4-dicarboxílico p-acedu ftálico |
C6H4(COOH)2 | 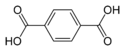
|
| Acedu truxílico | ácidu 2,4-difenilciclobutan-1,3-dicarboxílico | (C6H5)2C4H4(COOH)2 | 
|
| Acedu truxínico | ácidu 3,4-difenilciclobutan-1,2-dicarboxílico | (C6H5)2C4H4(COOH)2 | 
|
| Nome trivial | Estructura química | Δx | C:D | n−x |
|---|---|---|---|---|
| Ácidu acrílico | CH2=CH-COOH | - | 3:1 | n−1 |
| Acedu crotónico | CH3CH=CH-COOH | trans-Δ2 | 4:1 | n−2 |
| Acedu isocrotónico | CH3CH=CH-COOH | cis-Δ2 | 4:1 | n−2 |
| Ácidu sórbico | CH3CH=CH-CH=CH-COOH | trans,trans-Δ2,Δ4 | 6:2 | n−2 |
| Acedu undecilénico | CH2=CH(CH2)8COOH | - | 11:1 | n−1 |
| Acedu palmitoleico | CH3(CH2)5CH=CH(CH2)7COOH | cis-Δ9 | 16:1 | n−7 |
| Acedu sapiénico | CH3(CH2)8CH=CH(CH2)4COOH | cis-Δ6 | 16:1 | n−10 |
| Acedu oleico | CH3(CH2)7CH=CH(CH2)7COOH | cis-Δ9 | 18:1 | n−9 |
| Acedu eláidico | CH3(CH2)7CH=CH(CH2)7COOH | trans-Δ9 | 18:1 | n−9 |
| Acedu vaccénico | CH3(CH2)5CH=CH(CH2)9COOH | trans-Δ11 | 18:1 | n−7 |
| Acedu linoleico | CH3(CH2)4CH=CHCH2CH=CH(CH2)7COOH | cis,cis-Δ9,Δ12 | 18:2 | n−6 |
| Acedu linoeláidico | CH3(CH2)4CH=CHCH2CH=CH(CH2)7COOH | trans,trans-Δ9,Δ12 | 18:2 | n−6 |
| Acedu α-Linolénico | CH3CH2CH=CHCH2CH=CHCH2CH=CH(CH2)7COOH | cis,cis,cis-Δ9,Δ12,Δ15 | 18:3 | n−3 |
| Acedu ɣ-Linolénico | CH3(CH2)4CH=CHCH2CH=CHCH2CH=CH(CH2)4COOH | cis,cis,cis-Δ6,Δ9,Δ12 | 18:3 | n−6 |
| Acedu punícico | CH3(CH2)3CH=CH-CH=CH-CH=CH(CH2)7COOH | cis,trans,cis-Δ9,Δ11,Δ13 | 18:3 | n−5 |
| Acedu araquidónico | CH3(CH2)4CH=CHCH2CH=CHCH2CH=CHCH2CH=CH(CH2)3COOHNIST | cis,cis,cis,cis-Δ5Δ8,Δ11,Δ14 | 20:4 | n−6 |
| Acedu eicosapentaenoico | CH3CH2CH=CHCH2CH=CHCH2CH=CHCH2CH=CHCH2CH=CH(CH2)3COOH | cis,cis,cis,cis,cis-Δ5,Δ8,Δ11,Δ14,Δ17 | 20:5 | n−3 |
| Acedu erúcico | CH3(CH2)7CH=CH(CH2)11COOH | cis-Δ13 | 22:1 | n−9 |
| Acedu docosahexaenoico | CH3CH2CH=CHCH2CH=CHCH2CH=CHCH2CH=CHCH2CH=CHCH2CH=CH(CH2)2COOH | cis,cis,cis,cis,cis,cis-Δ4,Δ7,Δ10,Δ13,Δ16,Δ19 | 22:6 | n−3 |
Nel sistema IUPAC los nomes de los ácidos carboxílicos fórmense reemplazando la terminación “o” de los alcanos por “oico”, y anteponiendo la pallabra acedu.
La cadarma de los ácidos alcanoicos numbérase asignando'l N° 1 al carbonu carboxílico y siguiendo pola cadena más llarga qu'incluya'l grupu COOH.
Exemplu d'ácidos carboxílico complexu[editar | editar la fonte]
HOCH3-CH3-CH=CH-CH(CH3-CH=CH3)-CHBr-COOH
Nesti compuestu aparte del grupu funcional COOH, hai una función alcohol, pero d'alcuerdu a la so importancia y relevancia el grupu COOH ye'l principal; polo tanto'l grupu alcohol nomar como sustituyente. Polo tanto'l nome d'esti compuestu ye: Ácidu 3-alil-2-bromu-7-hidroxi-4-heptenoico.
La pallabra carboxi tamién s'utiliza pa nomar al grupu COOH cuando na molécula hai otru grupu funcional que tien prioridá sobre él.
Otros acedos carboxílicos importantes[editar | editar la fonte]
- Acedu benzoico
- Acedu láctico
- Acedu tartárico
- Acedu salicílico
- Acedu cafeico
- Acedu cinámico
- Ácidu cítrico
- Tolos aminoácidos contienen un grupu carboxilo y un grupu amino. Cuando reacciona'l grupu carboxilo d'un aminoácidu col grupu amino d'otru fórmase un enllaz amida llamáu enllaz peptídico. Les proteínes son polímeros d'aminoácidos y tienen nun estremu un grupu carboxilo terminal.
- Tolos ácidos grasos son acedos carboxílicos. Por casu, l'ácidu palmítico, esteárico, oleico, linoleico, etcétera. Estos ácidos cola glicerina formen ésteres llamaos triglicéridos.
- Los sales d'acedos carboxílicos de cadena llarga empléguense como tensoactivos.
Referencies[editar | editar la fonte]
- ↑ Wilhelm Riemenschneider “Carboxylic Acids, Aliphatic” in Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. doi 10.1002/14356007.a05_235 10.1002/14356007.a05_235.
- ↑ Vollhardt, K. Peter. Química Orgánica. 3ª edición. Añu 2000. Omega. Madrid. páxs. 849-850. ISBN 84-282-1172-8.


