Cinética enzimática

La cinética enzimática estudia la velocidá de les reacciones químiques que son catalizadas poles enzimes. L'estudiu de la Cinética y Mecanismos de Reacción cinética y de la dinámica química d'una enzima dexa esplicar los detalles del so mecanismu catalíticu, el so papel nel metabolismu, cómo ye controlada la so actividá na célula y cómo pue ser tornada la so actividá por fármacos o venenos o potenciada por otru tipu de molécules.
Les enzimes, na so mayoría, son proteínes cola capacidá de manipoliar otres molécules ensin ser alteriaos pola reacción,[1] eses molécules son denominaes sustratos. Un sustratu ye capaz de xunise al sitiu activu de la enzima que la reconoza y tresformase nun productu a lo llargo d'una serie de pasos denominaos mecanismu enzimáticu. Delles enzimes pueden xunir dellos sustratos distintos y/o lliberar diversos productos, como ye'l casu de les proteases al romper una proteína en dos polipéptidos. N'otros casos, produzse la unión simultánea de dos sustratos, como nel casu de l'ADN polimerasa, que ye capaz d'incorporar un nucleótido (sustratu 1) a una hebra d'ADN (sustratu 2). Anque toos estos mecanismos suelen siguir una complexa serie de pasos, tamién suelen presentar una etapa limitante que determina la velocidá final de tola reacción. Esta etapa limitante puede consistir nuna reacción química o nun cambéu conformacional de la enzima o del sustratu.
La conocencia adquirida alrodiu de la estructura de les enzimes foi de gran ayuda na visualización ya interpretación de los datos cinéticos. Por casu, la estructura puede suxurir cómo permanecen xuníos sustratu y productu mientres la catálisis, qué cambeos conformacionales asoceden mientres la reacción, o inclusive'l papel en particular de determinaes residuos aminoácidos nel mecanismu catalíticu. Delles enzimes modifiquen la so conformanza significativamente mientres la reacción, y nesi casu, pue ser crucial saber la estructura molecular de la enzima con y ensin sustratu xuníu (suélense usar análogos que se xunen pero nun dexen llevar a cabu la reacción y caltienen a la enzima permanentemente na conformanza de sustratu xuníu).
Los mecanismos enzimáticos pueden ser estremaos en mecanismu d'únicu sustratu o mecanismu de múltiples sustratos. Los estudios cinéticos llevaos a cabu n'enzimes que solo xunen un sustratu, como la triosafosfato isomerasa, pretenden midir l'afinidá cola que se xune'l sustratu y la velocidá cola que lo tresforma en productu. Per otru llau, al estudiar una enzima que xune dellos sustratos, como la dihidrofolato reductasa, la cinética enzimática puede amosar tamién l'orde nel que se xunen los sustratos y l'orde nel que los productos son lliberaos.
Sicasí, non toles catálisis biolóxiques son llevaes a cabu por enzimes proteiques. Esisten molécules catalítiques basaes nel ARN, como les ribozimes y los ribosomes, esenciales pal splicing alternativu y la traducción del ARNm, respeutivamente. La principal diferencia ente les ribozimas y les enzimes anicia nel llindáu númberu de reacciones que pueden llevar a cabu les primeres, anque los sos mecanismos de reacción y les sos cinétiques pueden ser estudiaes y clasificaes polos mesmos métodos.
Principios xenerales[editar | editar la fonte]

La reacción química catalizada por una enzima utiliza la mesma cantidá de sustratu y xenera la mesma cantidá de productu qu'una reacción non catalizada. Al igual qu'asocede n'otros tipos de catálisis, les enzimes nun alterien n'absolutu'l equilibriu de la reacción ente sustratu y productu.[2] La eficiencia de la reacción, hasta'l momentu en que tolos sitios posibles tean ocupaos. Nesi momentu algamaríase'l puntu de saturación de la enzima y, anque s'añedir más sustratu, nun va aumentar más la eficiencia de la mesma.
Ensayos enzimáticos[editar | editar la fonte]

Un ensayu enzimáticu ye un procedimientu, lleváu a cabu nun llaboratoriu, por aciu el cual puede midise la velocidá d'una reacción enzimática. Como les enzimes nun se peracaben na reacción que catalizan, los ensayos enzimáticos suelen midir los cambeos esperimentaos bien na concentración de sustratu (que va escayendo), bien na concentración de productu (que va aumentando). Esisten diversos métodos pa realizar estes midíes. La espectrofotometría dexa detectar cambeos na absorbancia de lluz per parte del sustratu o del productu (según la concentración d'estos) y la radiometría implica incorporación o lliberación de radioactividá pa midir la cantidá de productu llográu por tiempu. Los ensayos espectrofotométricos son los más utilizaos, yá que dexen midir la velocidá de la reacción de forma continua. Otra manera, los ensayos radiométricos riquen retirar les muestres pa midiles, polo que son ensayos discontinuos. Sicasí, estos ensayos son desaxeradamente sensibles y dexen detectar niveles bien baxos d'actividá enzimática.[3] Tamién puede utilizase la espectrometría de mases pa detectar la incorporación o lliberación d'isótopos estables cuando'l sustratu ye convertíu en productu. Anguaño esisten métodos senciellos que pueden emplegase con alumnos de bachilleratu como'l propuestu por Johnson R.J. y collaboradores,[4] quien empleguen hidrolasas de serina y un sustratu fluorogénico. Esti métodu ye rápido, sensible y dexa midir la cinética enzimática, al traviés de la xeneración de fluoresceína como productu.
Los ensayos enzimáticos más sensibles utilicen láseres dirixíos al traviés d'un microscopiu pa reparar los cambeos producíos n'enzimes individuales cuando catalizan una reacción. Estes midíes pueden utilizar cambeos producíos na fluorescencia de cofactores qu'intervienen nel mecanismu de catálisis o bien xunir molécules fluorescentes en llugares específicos de la enzima, que dexen detectar movimientos asocedíos mientres la catálisis.[5] Estos estudios tán dando una nueva visión de la cinética y la dinámica de les molécules individuales, n'oposición a los estudios de cinética enzimática tradicionales, nos que se repara y mídese el comportamientu d'una población de millones de molécules d'enzima.
Na figura de la derecha puede reparase la típica evolución d'una curva llograda nun ensayu enzimáticu. Primeramente, la enzima tresforma'l sustratu en productu siguiendo un comportamientu llinial. A midida que avanza la reacción, va escosándose la cantidá de sustratu y va menguando la cantidá de productu que se xenera por unidá de tiempu (mengua la velocidá de la reacción), lo que se manifiesta en forma de curva asintótica na gráfica. Dependiendo de les condiciones del ensayu y del tipu d'enzima, el periodu inicial puede durar dende milisegundos hasta hores. Los ensayos enzimáticos suelen tar estandarizados por que'l periodu inicial dure en redol a un minutu, pa llevar a cabu les midíes más fácilmente. Sicasí, los modernos equipos d'amiestu rápido de líquidos dexen llevar a cabu midíes cinétiques de periodos iniciales que la so duración puede aportar a inferior a un segundu.[6] Esti tipu d'ensayos rápidos son esenciales pa midíes de la cinética del estáu estacionariu, aldericada más embaxo.
La mayoría de los estudios de cinética enzimática centrar nel periodu inicial, esto ye, na zona llinial de la reacción enzimática. Sicasí, tamién ye posible midir tola curva de la reacción y afaer estos datos a una ecuación non llinial. Esta forma de midir les reacciones enzimáticas ye denominada analises de la curva de progresu.[7] Esti aproximamientu ye bien útil como alternativa a les cinétiques rápides, cuando'l periodu inicial ye demasiáu rápidu pa ser midíu con precisión.
Factores físicu-químicos que pueden modificar l'actividá enzimática[editar | editar la fonte]
- Temperatura: les enzimes son sensibles a la temperatura pudiendo trate modificada la so actividá por esti factor. Los rangos de temperatures óptimos pueden llegar a variar sustancialmente d'unes enzimes a otres. De normal, a midida que aumente la temperatura, una enzima va ver amontada la so actividá hasta'l momentu en qu'empiece la desnaturalización de la mesma, que va dar llugar a un amenorgamientu progresivu de dicha actividá.
- pH: el rangu de pH óptimo tamién ye bien variable ente distintes enzimes. Si'l pH del mediu alloñar del óptimo de la enzima, esta va ver modificada la so carga llétrica al aceptar o donar protones, lo que va modificar la estructura de los aminoácidos y por tanto l'actividá enzimática.
- Concentración salina: al igual que nos casos enantes mentaos, la concentración de sales del mediu ye crucial pa una óptima actividá enzimática. Una elevada concentración o una ausencia de sales nel mediu pueden torgar l'actividá enzimática, una y bones les enzimes precisen d'una fayadiza concentración d'iones pa caltener la so carga y la so estructura.
Reacciones con un sustratu[editar | editar la fonte]
Les enzimes que presenten un mecanismu d'únicu sustratu inclúin isomerases, tales como la triosafosfato isomerasa o la bisfosfoglicerato mutasa, y liases intramoleculares, tales como l'adenilato ciclasa o la ribozima ARN-liasa.[8] Sicasí, esisten ciertes reacciones enzimáticas d'únicu sustratu que nun pertenecen a esta categoría de mecanismos, como ye'l casu de la reacción catalizada pola catalasa. La catalasa reacciona primeramente con una molécula de peróxidu d'hidróxenu (agua osixenada) y queda nun estáu ferruñosu en lliberando'l productu (agua), y, darréu, ye amenorgada por una segunda molécula de sustratu. Anque mientres la reacción solo participa un sustratu, la esistencia d'un intermediariu enzimáticu modificáu dexa incluyir al mecanismu de la catalasa na categoría de mecanismos de ping-pong, un tipu de mecanismu aldericáu más palantre.
Cinética de Michaelis-Menten[editar | editar la fonte]
Como les reacciones catalizadas por enzimes son saturables, la velocidá de catálisis nun amuesa un comportamientu llinial nuna gráfica al aumentar la concentración de sustratu. Si la velocidá inicial de la reacción midir a una determinada concentración de sustratu (representáu como ), la velocidá de la reacción (representáu como ) aumenta linealmente col aumentu de la , como puede vese na figura. Sicasí, cuando aumentamos la , la enzima encher de sustratu y algama la so velocidá máxima , que nun va devasar en nengún casu, independientemente de la .

El modelu de cinética michaeliana pa una reacción d'únicu sustratu puede vese na figura de la izquierda. De primeres, tien llugar una reacción química bimolecular ente la enzima y el sustratu , formándose'l complexu enzima-sustratu . Anque'l mecanismu enzimáticu pa una reacción unimolecular puede ser bastante complexu, esiste una etapa enzimática limitante que dexa que'l mecanismu seya simplificáu como una etapa cinética única que la so constante ye .
- (Ecuación 1)
tamién llamáu o númberu de recambiu, fai referencia al máximu númberu de reacciones enzimáticas catalizadas per segundu.
A baxes concentraciones de sustratu, la enzima permanez nun equilibriu constante ente la forma llibre y el complexu enzima-sustratu . Aumentando la tamién aumentamos la por cuenta de la , moviendo l'equilibriu de la reacción escontra la derecha. Puesto que la velocidá de reacción depende de la , la velocidá ye sensible a pequeños cambeos na . Sicasí, a altes , la enzima encher y solo queda la forma xunida al sustratu . So estes condiciones, la velocidá de la reacción () dexa de ser sensible a pequeños cambeos na . Nesti casu, la concentración total d'enzima () ye aproximao igual a la concentración del complexu :

La ecuación de Michaelis-Menten[9] describe cómo la velocidá de la reacción depende del equilibriu ente la y la constante . Leonor Michaelis y Maud Menten demostraron que si ye enforma menor que (aproximamientu del equilibriu) puede deducise la siguiente ecuación:
- (Ecuación 2)
Esta famosa ecuación ye la base de la mayoría de les cinétiques enzimáticas de sustratu únicu.
La constante de Michaelis defínese como la concentración onde la velocidá de la reacción enzimática ye la metá de la . Esto puede verificase sustituyendo la concentración de sustratu por felicidá constante (). Si la etapa limitante de la velocidá de la reacción ye lenta comparada cola disociación de sustratu (), la constante de Michaelis va ser aproximao la constante de disociación del complexu , anque seya una situación relativamente rara.
La situación más común, onde , ye denominada cinética de Briggs-Haldane.[10] La ecuación de Michaelis-Menten entá se caltién so estes condiciones más xenerales, como puede derivase del aproximamientu del estáu estacionariu. Mientres el periodu inicial, la velocidá de la reacción ye más o menos constante, indicando que la tamién se va caltener constante:
D'esta forma, la concentración de vien dada pola siguiente espresión:
onde la constante de Michaelis defínese asina:
Colo cual, dempués d'operar tolos factores, llogramos una fórmula xeneral pa la velocidá de la reacción que coincide cola ecuación de Michaelis-Menten:
La constante d'especificidá mide la eficiencia cola qu'una enzima convierte un sustratu en productu. Utilizando la definición de la constante de Michaelis , la ecuación de Michaelis-Menten podría escribise de la siguiente forma:
onde ye la concentración d'enzima llibre. Asina, la constante d'especificidá convertir nuna constante bimolecular efeutiva de la enzima llibre que reacciona con sustratu llibre pa formar productu. Esta constante vien definida pola frecuencia cola que'l sustratu y l'enzima atopar nuna solución, y ronda aproximao un valor de 1010 M-1 s-1 a 25º C. Curiosamente, esti máximu nun depende del tamañu del sustratu o de la enzima. La proporción de les constantes d'especificidá pa dos sustratos ye una comparanza cuantitativa de la eficiencia de la enzima pa convertir en productos dichos sustratos. La rimada de la ecuación de Michaelis-Menten a baxes concentraciones de sustratu (cuando ) tamién apurre la constante d'especificidá.
Representación de la ecuación de Michaelis-Menten[editar | editar la fonte]

La gráfica de velocidá frente a amosada enantes nun ye llinial. Anque a baxes concentraciones de sustratu calténgase llinial, vase curvando a midida que aumenta la concentración de sustratu. Antes de la llegada de los ordenadores, que dexen afaer regresiones non lliniales de forma senciella, podía aportar a realmente difícil envalorar los valores de la y la nes gráfiques non lliniales. Esto dio llugar a que dellos investigadores concentraren los sos esfuercios en desenvolver linearizaciones de la ecuación de Michaelis-Menten, dando como resultáu la gráfica de Lineweaver-Burke y el diagrama de Eadie-Hofstee. Col siguiente tutorial de la cinética de Michaelis-Menten realizáu na Universidá de Virginia α, puede asemeyase el comportamientu d'una enzima variando les constantes cinétiques.
La gráfica de Lineweaver-Burk o representación de doble recíprocu ye la forma más común d'amosar los datos cinéticos. Pa ello, tómense los valores inversos a entrambos llaos de la ecuación de Michaelis-Menten. Como puede apreciase na figura de la derecha, la resultancia d'esti tipu de representación ye una llinia recta que la so ecuación ye , siendo'l puntu de corte ente la recta y l'exa d'ordenaes equivalente a , y el puntu de corte ente la recta y l'exa d'ascises equivalente a .
Obviamente, nun pueden tomase valores negativos pa ; el mínimu valor posible ye , que correspondería a una concentración infinita de sustratu, onde . El valor del puntu de corte ente la recta y l'exa x ye una extrapolación de datos esperimentales llograos en llaboratoriu. Xeneralmente, les gráfiques de Lineweaver-Burke aburuyen les midíes realizaes a baxes concentraciones de sustratu y esto puede dar llugar a estimaciones non bien exactes de la y de la .[11] Un modelu llinial muncho más exactu ye la diagrama de Eadie-Hofstee, pero nes investigaciones científiques actuales, tou esti tipu de linearizaciones quedaron obsoletos y fueron sustituyíos por métodos más fiables basaos n'analises de regresión non llinial. P'analizar los datos ye conveniente la normalización de los mesmos, una y bones esto puede ayudar menguando la cantidá de trabayu esperimental a realizar y amontando la fiabilidá del analís.[12]
Significáu de les constantes cinétiques[editar | editar la fonte]
La importancia del estudiu de la cinética enzimática mora en dos principios básicos. De primeres, dexa esplicar cómo funciona una enzima, y de segundes, dexa predicir cómo se va portar esa enzima in vivo. Les constantes cinétiques definíes enantes, y , son les pilastres fundamentales a la d'intentar entender el funcionamientu de les enzimes nel control del metabolismu. Asina, defínese como la velocidá máxima d'una reacción con una concentración d'enzima determinada () y como la concentración de sustratu necesaria p'algamar la metá de la velocidá máxima de la reacción.
Sicasí, llevar a cabu estes predicciones nun ye trivial, inclusive nos sistemes más simples. Por casu, la malato deshidrogenasa sintetiza, nel interior de la mitocondria, oxalacetato, que puede ser sustratu de diverses enzimes como la citrato sintasa, nel ciclu de los ácidos tricarboxílicos, la fosfoenolpiruvato carboxiquinasa, na gluconeogénesis, o l'aspartato aminotransferasa, na biosíntesis d'acedu aspártico. Pa ser capaz de predicir cuántu oxalacetato va ser esviáu por caúna de les rutes ye necesariu saber tantu la concentración del oxalacetato como la concentración y los parámetros cinéticos de caúna de les enzimes. Esti exemplu denota la complexidá que podemos llegar a atopar al intentar predicir el comportamientu de rutes metabóliques completes o d'organismos enteros, per mediu de modelos matemáticos. Anque estos oxetivos entá nun s'algamaron n'eucariotes, llográronse ciertos progresos en bacteries, utilizando modelos del metabolismu de Escherichia coli.[13][14]
Reacciones multisustrato[editar | editar la fonte]
Les reacciones multisustrato siguen una serie de complexes ecuaciones que describen cómo se xunen los sustratos y en qué orde lo faen. L'analís d'estes reacciones ye muncho más senciellu si la concentración del sustratu A caltiénse constante y la del sustratu B varia. Nestes condiciones, la enzima pórtase igual qu'una enzima d'únicu sustratu, polo que nuna gráfica de velocidá la concentración de sustratu va dar unos valores aparentes de les constantes cinétiques, Km y Vmax, pal sustratu B. Si realicen una serie de midíes a distintes concentraciones fixes de sustratu A, los datos llograos van dexar saber a qué tipu de mecanismu pertenez la reacción enzimática. Pa una enzima qu'una dos sustratos A y B, y tresformar en dos productos P y Q, esisten dos tipos de mecanismos descritos hasta agora.
Mecanismu de complexu ternariu[editar | editar la fonte]

Les enzimes (Y) que presenten esti mecanismu de reacción xunen coles mesmes los dos sustratos (A y B), dando llugar a un complexu ternariu EAB. L'orde secuencial d'unión de los sustratos puede ser al azar (mecanismu al azar) o siguir un orde en particular (mecanismu ordenáu). Si afitamos la concentración del sustratu A y variamos la de B, y representamos gráficamente'l comportamientu de la enzima por aciu un diagrama de Lineweaver-Burke, vamos llograr una serie de rectes con un puntu d'intersección común a toes elles.
Ente les enzimes que presenten esti mecanismu podemos atopar la glutation S-transferasa,[15] la dihidrofolato reductasa[16] y l'ADN polimerasa.[17] Los siguientes enllaces amuesen animaciones del mecanismu de complexu ternariu de la dihidrofolato reductasa β y del ADN polimerasa γ.
Mecanismu de ping-pong[editar | editar la fonte]
Como puede apreciase na figura de la derecha, les enzimes con un mecanismu de ping-pong pueden presentar dos estaos, la conformanza normal (Y) y la conformanza modificada químicamente (Y*) o conformanza entemedia. Nesti tipu de mecanismu, el sustratu A xúnese a la enzima Y, que pasa a un estáu entemediu Y*, por casu, por tresferencia d'un grupu químicu al centru activu de la enzima, pudiendo yá ser lliberáu en forma de productu P. Namái cuando'l sustratu A yá foi lliberáu del centru activu de la enzima puede xunise'l sustratu B, que devuelve a la enzima modificada Y* al so estáu orixinal Y, y lliberar en forma de productu Q. Si afitamos la concentración d'A y variamos la de B, y representamos gráficamente una enzima con mecanismu de ping-pong nun diagrama de Lineweaver-Burke, vamos llograr una serie de rectes paraleles ente sigo.

Ente les enzimes con esti tipu de mecanismu podemos atopar dalguna oxidorreductasa, como la tiorredoxima peroxidasa,[18] transferases, como l'acil-neuraminato citidil transferasa,[19] y serin proteasas, como la tripsina y la quimiotripsina.[20] Les serin-proteasas conformen una diversa familia d'enzimes bien comunes, qu'inclúin enzimes dixestives (tripsina, quimiotripsina y elastasa), delles enzimes del procesu de cuayamientu y munches otres. Nes serin-proteasas, l'estáu entemediu Y* ye una especie acilada nuna serina del centru catalíticu de la enzima. El siguiente enllaz amuesa una animación del mecanismu catalíticu de la quimiotripsina δ.
Cinétiques non Michaelianas[editar | editar la fonte]

Delles reacciones enzimáticas dan llugar a curves sigmoideas, al ser representaes nuna curva de saturación, lo que suel indicar una unión cooperativa del sustratu al centru catalíticu de la enzima. Esto quier dicir que la unión d'una molécula de sustratu inflúi na unión de les molécules de sustratu posteriores. Esti comportamientu ye'l más común nes enzimes multiméricas, que presenten delles zones d'interacción col sustratu.[21] El mecanismu de cooperación ye asemeyada al reparáu na hemoglobina. La unión d'una molécula de sustratu a una de les zones d'interacción alteria significativamente l'afinidá pol sustratu de les demás zones d'interacción. Les enzimes con esti tipu de comportamientu son denominaes alostéricas. La cooperatividad positiva tien llugar cuando la primer molécula de sustratu xunida amonta l'afinidá del restu de zones d'interacción. Otra manera, la cooperatividad negativa tien llugar cuando la primer molécula de sustratu xunida amenorga l'afinidá de la enzima por nuevu molécules de sustratu.
Como exemplos d'enzimes con cooperatividad positiva tenemos l'aspartato transcarbamilasa bacteriana[22] y la fosfofructoquinasa,[23] y con cooperatividad negativa, la tirosil ARNt-transferasa de mamíferos.[24]
La cooperatividad ye un fenómenu bastante común y puede aportar a crucial na regulación de la respuesta enzimática a cambeos na concentración de sustratu. La cooperatividad positiva fai que la enzima seya muncho más sensible a la concentración de sustratu, colo que la so actividá puede llegar a variar en gran midida anque se mueva en rangos bien estrechos de concentración de sustratu. Otra manera, la cooperatividad negativa fai que la enzima seya insensible a pequeños cambeos na concentración de sustratu.
La ecuación de Hill[25] suel ser utilizada pa describir cuantitativamente el grau de cooperatividad en cinétiques non michaelianas. El coeficiente de Hill (n) indica cuántes de les zones d'unión de sustratu d'una enzima afecten a l'afinidá de la unión del sustratu nel restu de les zones d'unión. El coeficiente de Hill puede tomar valores mayores o menores que 1:
- n < 1: indica cooperatividad negativa.
- n > 1: indica cooperatividad positiva.
Cinética del estáu preestacionario[editar | editar la fonte]

Al realizar un ensayu enzimáticu y entemecer la enzima col sustratu, esiste un curtiu periodu inicial nel que nun se produz nin síntesis de productu, nin estáu entemediu de la enzima. L'estudiu de los milisegundos siguientes al amiestu ye denomináu cinética del estáu preestacionario y ta rellacionáu cola formación y consumu de los intermediarios enzima-sustratu (YE o Y*) hasta'l momentu nel que s'algamar ciertes concentraciones y empieza l'estáu estacionariu.
La primer enzima na que s'estudió esti procesu, mientres la reacción d'hidrólisis, foi la quimiotripsina.[26] La detección d'intermediarios suel ser la principal evidencia necesaria pa saber so qué mecanismu actúa la enzima. Por casu, al realizar un ensayu de cinética rápida d'una reacción enzimática gobernada por un mecanismu de ping-pong, vamos poder faer un siguimientu de la lliberación de productu P y midir la formación d'intermediarios enzimáticos modificaos Y*.[27] Nel casu de la quimiotripsina, l'intermediariu enzimáticu producir por un ataque nucleofílico del sustratu sobre una serina del centru catalíticu, lo que xenera una forma intermediaria acilada de la quimiotripsina.
Na figura de la derecha, puede reparase como la enzima pasa rápido a un estáu entemediu Y* mientres los primeros segundos de la reacción. Darréu, cuando ye algamáu l'estáu estacionariu, la velocidá mengua. Esta primer fase de la reacción apurre la tasa de conversión de la enzima. Poro, la cantidá de productu lliberáu mientres esta fase (que puede llograse enllargando la recta correspondiente al estáu estacionariu hasta cortar la exa y) tamién da la cantidá d'enzima funcional presente nel ensayu.[28]
Mecanismu químicu[editar | editar la fonte]
Unu de los oxetivos más importantes nos estudios de la cinética enzimática ye determinar el mecanismu químicu que subyace na reacción enzimática, por casu, determinar la secuencia ordenada de sucesos que trescurren nel tresformamientu de sustratu en productu. Los aproximamientos cinéticos aldericaes enantes pueden apurrir información rellacionada cola velocidá de reacción de los intermediarios enzimáticos formaos, pero nun van dexar identificar qué intermediarios son esautamente.
Col fin de determinar la etapa limitante de la reacción o los intermediarios que se formen mientres la mesma, pueden llevase a cabu ensayo enzimáticos en diverses condiciones con enzimes o sustratos llixeramente modificaos, qu'apurran datos al respeutu. Un exemplu característicu d'etapa limitante d'una reacción ye aquella na que se ruempe un enllaz covalente dando llugar a un átomu d'hidróxenu. Si intercambiamos cada átomu d'hidróxenu pol so isótopu estable, deuteriu, vamos poder saber cual de los posibles hidróxenos tresferíos ye'l que determina la etapa limitante. La velocidá va sufrir una variación cuando l'hidróxenu críticu seya reemplazáu, debíu al efeutu isotópicu cinéticu primariu, que'l so orixe atopar na mayor estabilidá de les pontes de deuteriu, más difíciles de romper que les pontes d'hidróxenu.[29] Tamién ye posible midir efeutos similares per mediu d'otres sustituciones isotópiques, tales como 13C/12C ó 18O/16O, pero los efeutos producíos nestos casos son más difíciles de detectar.
Los isótopos tamién pueden ser utilizaos pa llograr información avera del destín de diverses partes de la molécula de sustratu cuando esti ye tresformáu en productu. Por casu, dacuando ye malo de determinar l'orixe d'un átomu d'osíxenu nel productu final, yá que puede provenir de l'agua o de la molécula de sustratu. Esto puede resolvese por aciu la sustitución sistemática de los átomos d'osíxenu de les molécules que participen na reacción, pol so isótopu estable 18O, llevando darréu a cabu una busca del isótopu nel productu llográu. El mecanismu químicu tamién puede ser elucidáu estudiando los efeutos cinéticos ya isotópicos baxu distintes condiciones de pH,[30] alteriando los niveles d'iones metálicos o otros cofactores,[31] por mutagénesis empobinada d'aminoácidos calteníos, o por aciu l'estudiu del comportamientu de la enzima en presencia d'análogos del sustratu.
Inhibición enzimática[editar | editar la fonte]

Los inhibidores enzimáticos son molécules qu'amenorguen o anulen l'actividá enzimática. Estos inhibidores pueden xunise a les enzimes de forma reversible (la desapaición del inhibidor restaura l'actividá enzimática) o irreversible (el inhibidor inactiva permanentemente a la enzima).
Inhibidores reversibles[editar | editar la fonte]
Los inhibidores enzimáticos reversibles pueden ser clasificaos como competitivos, acompetitivos, non competitivos y mistos, según l'efeutu que produzan nes constantes cinétiques Km y Vmax. Esti efeutu va depender de que'l inhibidor s'una a la enzima Y, al complexu enzima-sustratu YE o a dambos, como puede reparase na figura de la derecha y na tabla inferior. Pa clasificar correutamente un inhibidor pueden llevase a cabo estudio de la so cinética enzimática en función de la concentración de inhibidor. Los cuatro tipos de inhibición dan llugar a diagrames de Lineweaver-Burke y d'Eadie-Hofstee[11] que varien de distinta forma cola concentración de inhibidor. Pa embrivir, úsense dos símbolos:
- y
onde Ki y K'i son les constantes de disociación pa xunise a la enzima y al complexu enzima-sustratu, respeutivamente. En presencia d'un inhibidor reversible, los valores aparentes de la Km y la Vmax pasen a ser (α/α')Km y (1/α')Vmax, respeutivamente, como puede apreciase na tabla inferior pa los casos más comunes.
| Tipu de inhibición | Km aparente | Vmax aparente | ||
| solo Ki | () | competitiva |
align="center" | |
||
| solo Ki' | () | non competitiva |
align="center" | |
||
| Ki = Ki' | () | acompetitiva | ||
| Ki ≠ Ki' | () | mista |
align="center" | |
Los axustes por regresión non llinial de los datos de cinética enzimática[32] pueden apurrir estimaciones bien precises de les constantes de disociación Ki y Ki'.
Inhibidores irreversibles[editar | editar la fonte]
Los inhibidores enzimáticos tamién pueden xunise y inactivar una enzima de forma irreversible, xeneralmente per mediu de cambeos covalentes de residuos del centru catalíticu de la enzima. Estes reacciones aparren de forma esponencial y suelen ser saturables. Per debaxo de los niveles de saturación, caltienen una cinética de primer orde con respectu al inhibidor.
Mecanismos de catálisis[editar | editar la fonte]
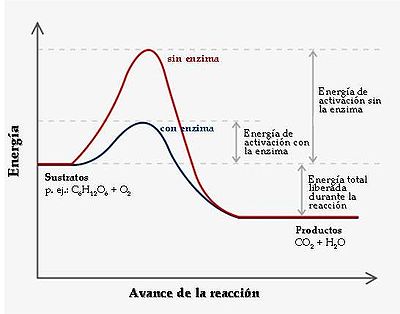
El modelu d'axuste inducíu ye'l más utilizáu al realizar estudios d'interacción enzima-sustratu.[33] Esti modelu propón que les interacciones iniciales ente la enzima y el sustratu son relativamente débiles, pero abondos pa producir ciertos cambeos conformacionales na enzima, qu'estabilicen y amonten la fuercia de la interacción. Estos cambeos conformacionales impliquen a una serie d'aminoácidos catalíticos del centru activu, nos cualos prodúcense los enllaces químicos correspondientes ente la enzima y el sustratu. Dempués de la unión, unu o más mecanismos de catálisis mengüen la enerxía del estáu de transición de la reacción, per mediu d'una ruta alternativa a la reacción. Los mecanismos de catálisis clasifiquen acorde a distintos criterios: catálisis covalente, catálisis por proximidá y alliniación d'orbitales, catálisis acedu-base xeneral, catálisis por iones metálicos y catálisis electrostática.
Los estudios de cinética enzimática nun dexen llograr el tipu de catálisis utilizada por una enzima. Sicasí, dellos datos cinéticos pueden apurrir una serie de nicios que lleven a realizar otru tipu d'estudios empobinaos a determinar dichu tipu de catálisis. Por casu, nun mecanismu de ping-pong la cinética del estáu pre-estacionariu pue tar suxuriendo una catálisis de tipu covalente. Per otru llau, variaciones nel pH pueden producir efeutos drásticos na Vmax pero non na Km, lo que podría indicar qu'una residuu del centru activu precisa un estáu concretu d'ionización por que pueda llevase a cabu la catálisis enzimática.
Catálisis enzimática[editar | editar la fonte]

La catálisis enzimática ye una disciplina de la enzimoloxía qu'estudia los mecanismos de catálisis polos cualos les proteínes o acedos nucleicos con actividá enzimática pueden favorecer la reacción de ciertos sustratos y la so conversión en productos. Esti fechu ta subordináu a les lleis de la catálisis química convencional: esto ye, la esistencia d'una enzima nun dexa l'apaición de nueves reacciones, nin va en contra de la termodinámica del procesu; a cencielles, acelera la so velocidá favoreciendo una ruta de menor costu enerxéticu incluyendo na dinámica de la reacción un tao intermediariu d'alta enerxía de cuenta que'l númberu de molécules actives, capaces de crear y destruyir nuevos enllaces, aumente.
Ver tamién[editar | editar la fonte]
Notes[editar | editar la fonte]
- α: Tutorial interactivo de la cinética enzimática de Michaelis–Menten (riqui Java)
- β: Mecanismu enzimáticu de la dihidrofolato reductasa (Gif)
- γ: Mecanismu enzimáticu del ADN-polimerasa (Gif)
- δ: Mecanismu enzimáticu de la quimiotripsina (rique Flash)
Referencies[editar | editar la fonte]
- ↑ Rodate, Beatriz (2013). Manual de práutiques de bioloxía molecular de la célula I. Facultá de Ciencies, UNAM.
- ↑ Ebbing, D.D. Xeneral chemistry
- ↑ Eisenthal R. Danson M.J. (Eds), Enzyme Assays: A Practical Approach. Oxford University Press (2002) ISBN 0-19-963820-9
- ↑ Johnson, R.J., Hoops, G.C., Savas, C.J., Kartje, Z., Lavis, L.D., A Sensitive and Robust Enzyme Kinetic Experiment Using Microplates and Fluorogenic Ester Substrates. Journal of Chemical Education. 2015; 92 (2), 385-388.
- ↑ Xie XS, Lu HP. Single-molecule enzymology. J Biol Chem. 1999 Jun 4;274(23):15967-70. PMID 10347141
- ↑ Gibson Q.H. Rapid mixing: Stopped flow Methods in Enzymology, (1969) 16:187-228
- ↑ Duggleby, R.G. Analysis of enzyme progress curves by non-linear regression. Methods in Enzymology, (1995) 249:61-90.
- ↑ Hammann C, Lilley DM. Folding and activity of the hammerhead ribozyme. Chembiochem. 2002 Aug 2;3(8):690-700. PMID 11779233
- ↑ Michaelis L. and Menten M.L. Kinetik der Invertinwirkung Biochem. Z. 1913; 49:333–369
- ↑ Briggs GUE, Haldane JB. A Note on the Kinetics of Enzyme Action. Biochem J. 1925;19(2):338-9. PMID 16743508
- ↑ 11,0 11,1 Tseng SJ, Hsu JP. A comparison of the parameter estimating procedures for the Michaelis–Menten model. J Theor Biol. 1990 Aug 23;145(4):457–64. PMID 2246896
- ↑ Bravo, I.G., Bustu, F., De Arriaga, D., Ferrero, M. A., Rodríguez-Aparicio, L. B., Martínez-Blanco H., Reglero, A. A normalised plot as a novel and time-saving tool in complex enzyme kinetic analysis Biochem. J. (2001). 358, 573-583. PMID 11577687
- ↑ Almaas Y, Kovacs B, Vicsek T, Oltvai ZN, Barabasi AL. Global organization of metabolic fluxes in the bacterium Escherichia coli. Nature. 2004 Feb 26;427(6977):839-43. PMID 14985762
- ↑ Reed JL, Vo TD, Schilling CH, Palsson BO. An expanded genome-scale model of Escherichia coli K-12 (iJR904 GSM/GPR). Genome Biol. 2003;4(9):R54. PMID 12952533
- ↑ Dirr H, Reinemer P, Huber R. X-ray crystal structures of cytosolic glutathione S-transferases. Implications for protein architecture, substrate recognition and catalytic function. Eur J Biochem. 1994 Mar 15;220(3):645-61. PMID 8143720
- ↑ Stone SR, Morrison JF. Dihydrofolate reductase from Escherichia coli: the kinetic mechanism with NADPH and reduced acetylpyridine adenine dinucleotide phosphate as substrates. Biochemistry. 1988 Jul 26;27(15):5493-9. PMID 3052577
- ↑ Fisher PA. Enzymologic mechanism of replicative DNA polymerases in higher eukaryotes. Prog Nucleic Acid Res Mol Biol. 1994;47:371-97. PMID 8016325
- ↑ Akerman SE, Muller S. 2-Cys peroxiredoxin PfTrx-Px1 is involved in the antioxidant defence of Plasmodium falciparum. Mol Biochem Parasitol. 2003 Aug 31;130(2):75-81. PMID 12946843
- ↑ Bravo, I.G., Barrallo, S., Ferrero, M. A., Rodríguez-Aparicio, L. B., Martínez-Blanco H., Reglero, A. “Kinetic properties of the Acylneuraminate Cytidylytransferase from Pasteurella haemolytica A2”. Biochem. J. (2001) 358, 585-598. [1]
- ↑ Kraut J. Serine proteases: structure and mechanism of catalysis. Annu Rev Biochem. 1977;46:331-58. PMID 332063
- ↑ Ricard J, Cornish-Bowden A. Co-operative and allosteric enzymes: 20 years on. Eur J Biochem. 1987 Jul 15;166(2):255-72. PMID 3301336
- ↑ Helmstaedt K, Krappmann S, Braus GH., Allosteric regulation of catalytic activity: Escherichia coli aspartate transcarbamoylase versus yeast chorismate mutara. Microbiol. Mol. Biol. Rev. 2001 Sep;65(3):404-21 PMID 11528003
- ↑ Schirmer T, Evans PR., Structural basis of the allosteric behaviour of phosphofructokinase. Nature. 1990 Jan 11;343(6254):140-5. PMID 2136935
- ↑ Ward WH, Fersht AR., Tyrosyl-tRNA synthetase acts as an asymmetric dimer in charging ARNt. A rationale for half-of-the-sites activity. Biochemistry. 1988 Jul 26;27(15):5525-30. PMID 3179266
- ↑ Hill, A. V. The possible effects of the aggregation of the molecules of haemoglobin on its dissociation curves. J. Physiol. (Lond.), 1910 40, iv-vii.
- ↑ Hartley B.S. and Kilby B.A. The reaction of p-nitrophenyl esters with chymotrypsin and insulin. Biochem J. 1954 Feb;56(2):288-97. PMID 13140189
- ↑ Alan Fersht, Structure and Mechanism in Protein Science: A Guide to Enzyme Catalysis and Protein Folding. W. H. Freeman, 1998. ISBN 0-7167-3268-8
- ↑ Bender ML, Begue-Canton ML, Blakeley RL, Brubacher LJ, Feder J, Gunter CR, Kezdy FJ, Killheffer JV Jr, Marshall TH, Miller CG, Roeske RW, Stoops JK. The Determination of the Concentration of Hydrolytic Enzyme Solutions: a-Chymotrypsin, Trypsin, Papain, Elastase, Subtilisin, and Acetylcholinesterase. J Am Chem Soc. 1966 Dec 20;88(24):5890-913. PMID 5980876
- ↑ Cleland WW. The use of isotope effects to determine enzyme mechanisms. Arch Biochem Biophys. 2005 Jan 1;433(1):2-12. PMID 15581561
- ↑ Cleland WW. Use of isotope effects to elucidate enzyme mechanisms. CRC Crit Rev Biochem. 1982;13(4):385-428. PMID 6759038
- ↑ Christianson DW, Cox JD. Catalysis by metal-activated hydroxide in cinc and manganese metalloenzymes. Annu Rev Biochem. 1999;68:33-57. PMID 10872443
- ↑ Leatherbarrow RJ. Using linear and non-linear regression to fit biochemical data. Trends Biochem Sci. 1990 Dec;15(12):455–8. PMID 2077683
- ↑ Koshland DE, Application of a Theory of Enzyme Specificity to Protein Synthesis. Proc. Natl. Acad. Sci. U.S.A. 1958 Feb;44(2):98-104. PMID 16590179
Pa más información[editar | editar la fonte]
- Athel Cornish-Bowden, Fundamentals of Enzyme Kinetics. (3rd edition), Portland Press 2004, ISBN 1-85578-158-1.
- Irwin H. Segel, Enzyme Kinetics: Behavior and Analysis of Rapid Equilibrium and Steady-State Enzyme Systems. Wiley-Interscience; New Ed edition 1993, ISBN 0-471-30309-7.
- Alan Fersht, Structure and Mechanism in Protein Science: A Guide to Enzyme Catalysis and Protein Folding. W. H. Freeman, 1998. ISBN 0-7167-3268-8
- Santiago Schnell, Philip K. Maini, A century of enzyme kinetics: Reliability of the KM and vmax estimates, Comments on Theoretical Biology 8, 169-187, 2004 DOI: 10.1080/08948550390206768
- Chris Walsh, Enzymatic Reaction Mechanisms. W. H. Freeman and Company. 1979. ISBN 0-7167-0070-0
- Nicholas Price, Lewis Stevens, Fundamentals of Enzymology, Oxford University Press, 1999. ISBN 0-19-850229-X
- Tim Bugg, An Introduction to Enzyme and Coenzyme Chemistry Blackwell Publishing, 2004 ISBN 1-4051-1452-5
Enllaces esternos[editar | editar la fonte]
- Animación d'un ensayu enzimáticu
- MACiE: Base de datos de mecanismos de reacciones enzimáticas
- ENZYME(Expasy): Base de datos de nomenclatura enzimática
- ExCatDB: Base de datos de mecanismos catalíticos enzimáticos
- BRENDA: Base de datos sobre rutes enzimáticas, onde s'amuesen diagrames de reacción, sustratos y productos de les reacciones
- SABIU-RK: Base de datos de reacciones cinétiques
- Joseph Kraut's Research Group, University of California San Diego: Animaciones de delles reacciones enzimáticas
- Simboloxía y Terminoloxía de la cinética enzimática
- Introducción a la cinética enzimática

![{\displaystyle {\rm {[S]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/296314b84c6c87e93144cf168e34db7d62e5876e)







![{\displaystyle {\begin{matrix}v=k_{2}[{\mbox{YE}}]\end{matrix}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/97a9501d94ac1d8fec82d7c0dff552075641f008)

![{\displaystyle {\rm {[YE]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9aa1fe1db185779ae2a023992f3dea0547bb5d88)
![{\displaystyle {\rm {[Y]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/218878eba8f59a25aa9b2c31072b453f38a9a3f5)
![{\displaystyle v\approx k_{2}\mathrm {[Y]_{tot}} =V_{\rm {max}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1b82c627306d9220ccdd0c83a015a43f604d4e68)
![{\displaystyle {\rm {[Y]_{tot}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/210968b428db76db068178f543e4ce407f965012)
![{\displaystyle [{\mbox{Y}}]_{\rm {tot}}\ {\stackrel {\mathrm {def} }{=}}\ [{\mbox{Y}}]+[{\mbox{YE}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/908b638d7968ee5b6753dbbef1ff99b1c4411fcd)

![{\displaystyle v={\frac {V_{\rm {max}}[{\mbox{S}}]}{K_{\rm {m}}+[{\mbox{S}}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/adbc2701aefc76c152483244c40ef41f9568abd5)

![{\displaystyle \mathrm {[S]} =K_{\rm {m}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/497c50c4e4fb56de42d92f486816452b451cafdc)


![{\displaystyle {\frac {\mathrm {d} }{\mathrm {d} t}}[{\mbox{YE}}]=k_{1}[{\mbox{Y}}][{\mbox{S}}]-k_{2}[{\mbox{YE}}]-k_{-1}[{\mbox{YE}}]\approx 0}](https://wikimedia.org/api/rest_v1/media/math/render/svg/06cae360018c6cb1e57019810af487f151f5e4ee)
![{\displaystyle [{\mbox{YE}}]\approx {\frac {[{\mbox{Y}}]_{\rm {tot}}[{\mbox{S}}]}{[{\mbox{S}}]+K_{\rm {m}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a76184c038fca74f4c083df14e184e2e33f830a6)
![{\displaystyle K_{\rm {m}}\ {\stackrel {\mathrm {def} }{=}}\ {\frac {k_{2}+k_{-1}}{k_{1}}}\approx {\frac {[{\mbox{Y}}][{\mbox{S}}]}{[{\mbox{YE}}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2c4d08ae93d689947f6e7eaea3a6a22c38812c5b)
![{\displaystyle v=k_{2}[\mathrm {YE} ]={\frac {k_{2}[{\mbox{Y}}]_{\rm {tot}}[{\mbox{S}}]}{[{\mbox{S}}]+K_{\rm {m}}}}={\frac {V_{\rm {max}}[{\mbox{S}}]}{[{\mbox{S}}]+K_{\rm {m}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9a288d9951fe05d97c1062de98a0efb632768798)

![{\displaystyle v=k_{2}[\mathrm {YE} ]={\frac {k_{2}}{K_{\rm {m}}}}[{\mbox{Y}}][{\mbox{S}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d7443103a4721366ad0e8022db04ef4ff56de7c0)
![{\displaystyle \mathrm {[S]} \ll K_{\rm {m}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/68dbd7813d5ed06a1a1f7a51c3be98e68549b5fc)



![{\displaystyle {\frac {1}{v}}={\frac {K_{\rm {m}}}{V_{\rm {max}}[{\mbox{S}}]}}+{\frac {1}{V_{\rm {max}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d612f259c3edae899518d9f4e7f65eb4e02e49b3)
![{\displaystyle 1/\mathrm {[S]} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/57cb5878d583ce6b4d7181c44a4feea01b611add)
![{\displaystyle 1/\mathrm {[S]} =0}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6808a7f92793d6a6753256c39f7f9c16f758307d)


![{\displaystyle \alpha =1+{\frac {[{\mbox{I}}]}{K_{i}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7d05bffbc19ef9047581c87887ae0eea5c11e7fe)
![{\displaystyle \alpha ^{\prime }=1+{\frac {[{\mbox{I}}]}{K_{i}^{\prime }}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e8b2033b5725a8b85d7425d409192cf11885c199)









