Éster
| Éster | |
|---|---|
|
clase estructural de compuestos químicos (es) | |
|
organooxygen compound (en) | |

Los ésteres son compuestos orgánicos derivaos de petroleu o inorgánicos osixenaos nos cualos unu o más protones son sustituyíos por grupos orgánicos arriendo (simbolizaos por R').
Etimológicamente, la pallabra "éster" provién del alemán Yesig-Äther (éter de vinagre), como se llamaba d'antiguo al acetato de etilo.[1]
Descripción
[editar | editar la fonte]Nos ésteres más comunes l'ácidu en cuestión ye un acedu carboxílico. Por casu, si l'ácidu ye'l acedu etanoico o acético, el éster ye denomináu como etanoato o acetato. Los ésteres tamién pueden formase con ácidos inorgánicos, como l'ácidu carbónico (anicia ésteres carbónicos), l'ácidu fosfórico (ésteres fosfóricos) o'l ácidu sulfúrico. Por casu, el sulfatu de dimetilo ye un éster, dacuando llamáu "éster dimetílico del ácidu sulfúrico".
| Éster (éster d'ácidu carboxílico) |
Éster carbónicu (éster d'ácidu carbónico) |
Éster fosfóricu (triéster d'ácidu fosfórico) |
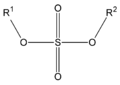
Éster sulfúricu (diéster d'ácidu sulfúrico) |
|---|---|---|---|

|

|

|
|
Un ensayu recomendable pa detectar ésteres ye la formación de hidroxamatos férricos, fáciles de reconocer yá que son bien coloriaos:
Ensayu del ácidu hidroxámico: la primer etapa de la reacción ye la conversión del éster nun ácidu hidroxámico (catalizado por base). Nel siguiente pasu ésti reacciona con tricloruro de fierro produciendo un hidroxamato d'intensu color coloráu-violeta.
En bioquímica son el productu de la reacción ente los ácidos grasos y los alcoholes.
Na formación de ésteres, cada radical -OH (grupu hidroxilo) del radical del alcohol sustituyir pola cadena -COO del ácidu grasu. El H sobrante del grupu carboxilo, combinar col OH sustituyíu, formando agua.
En química orgánica y bioquímica los ésteres son un grupu funcional compuestu d'un radical orgánicu xuníu a la residuu de cualesquier ácidu osixenáu, orgánicu o inorgánicu. Los ésteres más comúnmente atopaos na naturaleza son les grases, que son ésteres de glicerina y ácidos grasos (acedu oleico, acedu esteárico, etc.)
Principalmente resultante de la condensación d'un acedu carboxílico y un alcohol. El procesu denominar esterificación. Un éster cíclicu ye una lactona.

Nomenclatura
[editar | editar la fonte]
La nomenclatura de los ésteres deriva del ácidu carboxílico y l'alcohol de los que procede. Asina, nel etanoato (o acetato) de metilu atopamos dos partes nel so nome:
- La primer parte del nome, etanoato (o acetato), provién del acedu etanoico (acético).
- La otra metá, de metilu, provién del alcohol metílico (metanol).
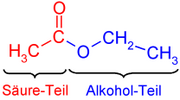
Nel dibuxu de la derecha repara la parte que procede del ácidu (en colloráu; etanoato) y la parte que procede del alcohol (n'azul, de etilo).
Depués el nome xeneral d'un éster d'ácidu carboxílico va ser "alcanoato d'arriendo" onde:
- alcan-= raigañu de la cadena carbonada principal (si ye un alcano), que se noma a partir del númberu d'átomos de carbonu. Por casu:propan- significa cadena de 3 átomos de carbonu xuníu por enllaces senciellos.
- oato = sufixu qu'indica que ye deriváu d'un ácidu carboxílico. Por casu: propanoato: CH3-CH2-COO- significa "deriváu del ácidu propanoico".
- d'arriendo: Indica l'alcohol de procedencia. Por casu: -O-CH2-CH3 ye "de etilo"
En xunto CH3-CH2-COO-CH2-CH3 nómase propanoato de etilo.
Propiedaes físiques
[editar | editar la fonte]Los ésteres pueden participar nos enllaces d'hidróxenu como aceptadores, pero nun pueden participar como apurridores nesti tipu d'enllaces, a diferencia de los alcoholes de los que deriven. Esta capacidá de participar nos enllaces d'hidróxenu conviérte-yos en más hidrosolubles que los hidrocarburos de los que deriven. Pero les llimitaciones de los sos enllaces d'hidróxenu facer más hidrofóbicos que los alcoholes o ácidos de los que deriven. Esta falta de capacidá d'actuar como apurridor d'enllaz d'hidróxenu causa que nun puedan formar enllaces d'hidróxenu ente molécules de ésteres, lo que los fai más volátiles qu'un ácidu o alcohol de similar pesu molecular.
Munchos ésteres tienen un arume carauterístico, lo que fai que s'utilicen llargamente como sabores y arumes artificiales. Por casu:
- Acetato de 2-etilhexilo: sabor a dulzuxu nidiu
- butanoato de metilu: sabor a Piña
- salicilato de metilu (aceite de siempreverde o menta): arume de les pomaes Germolene™ y Ralgex™ (Reinu Xuníu)
- octanoato de heptilo: sabor a artimora
- etanoato de isopentilo: sabor a plátanu
- pentanoato de pentilo: sabor a mazana
- butanoato de pentilo: sabor a pera o a albaricoque
- etanoato de octilo: sabor a naranxa.
Los ésteres tamién participen na hidrólisis esterárica: la rotura d'un éster por agua. Los ésteres tamién pueden ser descompuestos por ácidos o bases fuertes. Como resultancia, descomponer nun alcohol y un acedu carboxílico, o una sal d'un ácidu carboxílico:

Propiedaes químiques
[editar | editar la fonte]Nes reacciones de los ésteres, la cadena ruémpese siempres nun enllaz senciellu, yá sía ente l'osíxenu y l'alcohol o R, yá sía ente l'osíxenu y el grupu R-CO-, esaniciando asina l'alcohol o unu de los sos derivaos. La saponificación de los ésteres, llamada asina pola so analoxía cola formación de xabones, ye la reacción inversa a la esterificación.
Los ésteres se hidrogenan más fácilmente que los ácidos, emplegándose xeneralmente'l éster etílicu tratáu con un amiestu de sodiu y alcohol (Amenorgamientu de Bouveault-Blanc). L'hidruru de litiu y aluminiu amenorga ésteres d'acedos carboxílicos pa dar 2 equivalentes d'alcohol.[2] La reacción ye d'ampliu espectru y utilizóse p'amenorgar diversos ésteres. Les lactonas producen dioles. Esisten diversos axentes reductores alternativos al hidruru de litiu y aluminiu como'l DIBALH, el trietil-borohidruro de litiu o BH3–SiMe3 a refluxu con THF.[3]
El dicloruro de titanoceno amenorga los ésteres d'acedos carboxílicos hasta'l alcano (RCH3)y l'alcohol R-OH.[4] El mecanismu probablemente débese a la formación d'un alqueno intermediariu.

L'hidróxenu α de munchos ésteres puede ser sustraíu con una base non nucleofílica o'l alcóxido correspondiente al éster. El carbanión xeneráu puede xunise a diversos sustratos en diverses reacciones de condensación, tales como la condensación de Claisen, la condensación de Dieckmann y la síntesis malónica. Munchos métodos de síntesis d'aniellos heterocíclicos aprovechen estes propiedaes químiques de los ésteres, tales como la síntesis de pirroles de Hantzsch y la síntesis de Feist-Benary.
Esisten reacciones de condensación nes que s'utiliza un reductor qu'apurra electrones pa formar l'enllaz C-C ente grupos acilo, como'l casu de la condensación aciloínica. Los ésteres pueden dar alcoholes con dos sustituyentes idénticos por adición de reactivos de Grignard. Unes aplicación d'esta reacción ye la reacción de Fujimoto-Belleau.
Referencies
[editar | editar la fonte]
