Electrólisis
La electrólisis ye'l procesu que dixebra los elementos d'un compuestu per mediu de la lletricidá. Nella asocede la captura d'electrones polos cationes nel cátodu (un amenorgamientu) y la lliberación d'electrones polos aniones nel ánodu (una oxidación).
Historia[editar | editar la fonte]
Foi afayada por fuercia en 1800 por William Nicholson mientres estudiaba'l funcionamientu de les bateríes. En 1834 el físicu y químicu inglés Michael Faraday desenvolvió y publicó les lleis de la electrólisis que lleven el so nome y acuñó los términos.
Procesu[editar | editar la fonte]

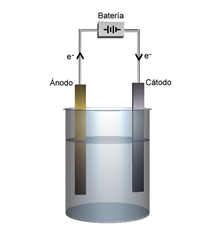
- Aplícase una corriente llétrica continua por aciu un par d'electrodos coneutaos a una fonte d'alimentación llétrico y somorguiaos na disolución. L'electrodu coneutáu al polu positivu conozse como ánodu, y el coneutáu al negativu como cátodu.[1]
- Cada electrodu atrai a los iones de carga opuesta. Asina, los iones negativos, o aniones, son atraíos y muévense escontra l'ánodu (electrodu positivu), ente que los iones positivos, o cationes, son atraíos y muévense escontra'l cátodu (electrodu negativu).
- La manera más fácil de recordar toa esta terminoloxía ye afitándose nel raigañu griegu de les pallabres. Odos significa camín. Electrodu ye'l camín pol que van los electrones. Catha significa escontra baxo (catacumba, catástrofe). Cátodu ye'l camín por onde cayen los electrones. Anas significa escontra riba. Ánodu ye'l camín pol que xuben los electrones. Ion significa caminante. Anión dirixir al ánodu y catión dirixir al cátodu. La nomenclatura utilízase tamién en piles. Una forma fácil tamién de recordar la terminoloxía ye teniendo en cuenta la primer lletra de cada electrodu y acomuñar al procesu que nél asocede; esto ye: nel ánodu produz la oxidación (los dos pallabres empiecen con vocales) y nel cátodu l'amenorgamientu (los dos pallabres empiecen con consonantes).
- La enerxía necesaria pa dixebrar a los iones y amontar la so concentración nos electrodos ye apurrida pola fonte d'alimentación llétrico.
- Nos electrodos produz una tresferencia d'electrones ente estos y los iones, produciéndose nueves sustancies. Los iones negativos o aniones dexen electrones al ánodu (+) y los iones positivos o cationes tomen electrones del cátodu (−).
En definitiva lo qu'asocede ye una reaición d'oxidación-amenorgamientu, onde la fonte d'alimentación llétrico encargar d'apurrir la enerxía necesaria.
Electrólisis de l'agua[editar | editar la fonte]
Si l'agua nun ye destilada, la electrólisis non yá dixebra l'osíxenu y l'hidróxenu, sinón los demás componentes que tean presentes como sales, metales y dellos otros minerales (lo que fai que l'agua conduza la lletricidá nun ye'l H2O, sinón que son los minerales. Si l'agua tuviera destilada y fora 100% pura, nun tendría conductividá).
Ye importante faer delles considerancies:
- Nunca tienen de xunise los electrodos, una y bones la corriente llétrica nun va consiguir el procesu y la batería se sobrecalentará y va quemar.
- Tien De utilizase siempres corriente continua (enerxía de bateríes o d'adaptadores de corriente), nunca corriente alterna (enerxía del enchufe de la rede).
- La electrólisis tien de faese de tal manera que los dos gases desprendíos nun entren en contautu, de lo contrario produciríen un amiestu peligrosamente esplosiva (una y bones l'osíxenu y l'hidróxenu resultantes atópase en proporción estequiométrica).
- Una manera de producir agua otra vegada, ye por aciu la esposición a un catalizador. El más común ye'l calor; otru ye'l platín en forma de llana fino o polvu. El segundu casu tien de faese con muncho curiáu, incorporando cantidaes pequeñes d'hidróxenu en presencia d'osíxenu y el catalizador, de manera que l'hidróxenu quémese selemente, produciendo una llapada tenue. Lo contrario nunca tien de faese ensin debida investigación y ayuda profesional.
Aplicaciones de la electrólisis[editar | editar la fonte]


- Produición d'aluminiu, litiu, sodiu, potasiu, y magnesiu.
- Produición de hidróxidu de sodiu, ácidu clorhídrico, cloratu de sodiu y cloratu de potasiu.
- Produición d'hidróxenu con múltiples usos na industria: como combustible, en soldadures, etc. Ver más n'hidróxenu diatómico.
- La electrólisis d'una solución salina dexa producir hipoclorito (cloru): esti métodu emplegar pa consiguir una cloración ecolóxica de l'agua de les piscines.
- La electrometalurgia ye un procesu pa dixebrar el metal puro de compuestos usando la electrólisis. Por casu, l'hidróxidu de sodiu ye dixebráu en sodiu puru, osíxenu puro ya hidróxenu puru.
- L'anodización ye usada pa protexer los metales del escomiu.
- La galvanoplastia, tamién usada pa evitar l'escomiu de metales, crea una película delgada d'un metal menos corrosible sobre otru metal.
Referencies[editar | editar la fonte]
Enllaces esternos[editar | editar la fonte]
 Wikimedia Commons tien conteníu multimedia tocante a Electrólisis.
Wikimedia Commons tien conteníu multimedia tocante a Electrólisis.
