Compuestu de organosilicio

Los compuestos orgánicos de siliciu o compuestos de organosilicio son compuestos orgánicos que contienen enllaces covalentes ente átomos de carbonu y de siliciu. La química de organosilicio ye la caña de la química qu'estudia les sos propiedaes y reactividá.[1]
Como'l carbonu, el siliciu xunío con enllaces covalentes a sustituyentes orgánicos ye tetravalente y la so estructura ye tetraédrica. Polo xeneral, enllazar siliciu-carbonu nun tán presentes nos procesos bioquímicos,[2] anque hai informes de la so esistencia efímera nun alga d'agua duce.[3] El primer compuestu orgánicu de siliciu conocíu, el tetraetilsilano, foi afayáu por Charles Friedel y James Crafts en 1863 por reacción de tetraclorosilano con dietilzinc. Como esceición, el carburu de siliciu ye un compuestu inorgánicu.
Organosilanos[editar | editar la fonte]
Enllazar carbonu - siliciu son más llargos en comparanza colos enllaces carbonu-carbonu (llargor d'enllaz de 186 pm vs 154 pm) y son más débiles, con una enerxía de disociación del enllaz de 451 kJ/mol frente a 607 kJ/mol.[4] L'enllaz C-Si ta daqué polarizáu escontra'l carbonu por cuenta del so mayor electronegatividá (C=2,55 vs Si=1,90). Una manifestación de la polaridá d'estos enllaces nos organosilanos atópase na reacción de Sakurai. Los acoplamientos oxidativos del siliciu ta representaos pol acoplamientu de Hiyama. Ciertos silanos d'arriendo pueden ser aferruñaos pa dar un alcohol como na oxidación de Fleming-Tamao.
Ciertos silanos de alilo pueden ser preparaos a partir d'un éster alílico (como'l compuestu 1) y de monosililcobre (como'l 2).[5][6]
Nesta reacción inviértese la polaridá habitual del siliciu nun enllaz químicu col cinc y tien llugar una sustitución alílica formal del grupu benzoiloxi.
La química de los silanos como'l tetrametilsilano ye comparable a la de los alcanos en munchos aspeutos tales como la estabilidá térmica. L'efeutu β-siliciu describe l'efeutu estabilizador d'un átomu de β-siliciu nun carbocatión, lo cual trai munches implicaciones pa la reactividá.
Silóxidos[editar | editar la fonte]
Hai que resaltar que los enllaces siliciu - osíxenu son muncho más curtios y más fuertes (809 frente a 538 kJ/mol) que los enllaces carbonu - osíxenu. La polaridá d'esti enllaz aumenta escontra l'osíxenu. Exemplos d'ello son los acetales de sililo RR'Si(OR)2, los silanoles, los siloxanos y el polímeru polisiloxano. Los sililéteres son utilizaos como grupos proteutores de los alcoholes. Namái los enllaces siliciu - flúor son más fuertes que los enllaces carbonu - flúor y ye por eso que la fonte de flúor TASF (o, más davezu'l TBAF) son útiles na desprotección. La formación favorable d'enlace Si-O conduz a munches reacciones orgániques como'l reordenamientu de Brook y la olefinación de Peterson.
Otra manifestación ye la naturaleza altamente esplosiva de los grupos pendientes con siliciu, Si(CH2ONO2)4 y Si(CH2N3)4, del tetranitrato de pentaeritritol:[7][8]
Un únicu cristal d'esti compuestu, sintetizáu per primer vegada en 2007, españa inclusive cuando se pon en contautu con una espátula de teflón y, ello ye que foi imposible la so completa carauterización. Otru factor que contribúi a la so descomposición exotérmica (deducida de la esperimentación muncho más segura in silico) ye la capacidá del siliciu na so fase de cristal pa coordinase con dos grupos de nitrito d'osíxenu, amás de la so coordinación regular colos cuatro átomos de carbonu. Esta coordinación adicional fadría más fácil la formación del dióxidu de siliciu (unu de los productos de descomposición).
Haluros de sililo[editar | editar la fonte]
Los haluros de organosililo son reactivos importantes en química orgánicasobremanera'l cloruru de trimetilsililo Me3SiCl. Un métodu clásicu llamáu reacción de Flood pa la síntesis d'esti tipu de compuestos ye por calentamientu de hexaalquildisiloxanos R3SiOSiR3 con ácidu sulfúrico concentráu y un haluru de sodiu.[9] Otros haluros de sililo relevantes son: diclorometilfenilsilano, dimetildiclorosilano,metiltriclorosilano, (4-aminobutil)dietoximetilsilano, tricloro(clorometil)silano , tricloro(diclorofenil)silano, tricloroetilsilano, triclorofenilsilano y trimetilclorosilano.
Hidruros de sililo[editar | editar la fonte]
L'enllaz siliciu - hidróxenu ye más llargu que l'enllaz C-H (148 frente a 105 pm de llargor d'enllaz) y ye más débil (299 frente a 338 kJ/mol d'enerxía d'enllaz). L'hidróxenu ye más electronegativu que'l siliciu y de ende la convención de nomenclatura d'hidruru de sililo (al igual que'l grupu metilu que deriva del metanu). El compuestu d'orixe SiH4 llámase silano, y unu de los sos derivaos ye'l fenilsilano. Los hidruros de sililo son bien reactivos y utilícense como axentes reductoress, por casu, PMHS.
Nun estudiu'l trietilsililo utilizar na conversión d'un fenilazida nun anilina:[10]
Nesta reacción l'ACCN ye un iniciador de radicales y un tiol alifático tresfier el calter radical al hidruru de sililo. El radical llibre trietilsililo reacciona depués cola azida con espulsión de nitróxenu a un radical N-sililarilaminilo que abstrae un protón d'un tiol pa completar asina'l ciclu catalíticu:
El tratamientu final con agua produz la anilina.
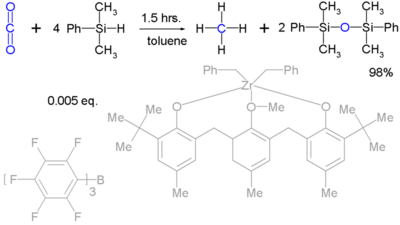
Los hidruros de sililo pueden inclusive producir hasta l'amenorgamientu de molécules bien estables como dióxidu de carbonu (pa dar metanu):[11]
Anque ello precisa un sistema catalizador bien complexu.
Hidrosililación[editar | editar la fonte]
Los hidruros de sililo reaccionen con distintos sustratos insaturados como alquenos, alquinos, imines, carbonilos y oximes dando nuevos compuestos orgánicos de siliciu nun procesu llamáu hidrosililación. Na reacción d'hidruru de trifenilsililo con fenilacetileno el productu de reacción ye un isómero trans o cis, o'l vinilsilano geminal, por casu:[12] trans
Na sililmetalación rellacionada, un metal reemplaza al átomu d'hidróxenu.
Silenos[editar | editar la fonte]
Los compuestos orgánicos de siliciu, a diferencia de los sos homólogos de carbonu, nun tener una rica química del doble enllaz por cuenta de la gran diferencia de electronegatividá.[13] Los compuestos esistentes con enllaces silenu Si=C (tamién conocíos como alquilidensilanos) son intereses de llaboratoriu, tales como l'análogu del bencenu con átomos de siliciu silabenceno. En 1967, L. Y. Gusel'Nikov y M. C. Flowers apurrieron la primer evidencia de la esistencia de los silenos a partir de la pirólisis del dimetilsilaciclobutano.[14] El primer silenu estable (cinéticamente blindáu) foi afayáu en 1981 por Brook.[15]
Los disilenos tienen doble enllace Si=Si y los disilinos son análogos d'un alquino con siliciu. El primer silino (con un triple enllaz ente siliciu y carbonu, Si≡C) foi informáu en 2010.
Siloles[editar | editar la fonte]

Los siloles, tamién llamáusilaciclopentadienos, son miembros d'una clase más amplia de compuestos llamaos metaloles,[16] son los análogos de los pirroles con siliciu y son d'actual interés académicu por cuenta del so electroluminiscencia y otres propiedaes electróniques.[17][18] Los siloles son eficientes nel tresporte d'electrones. Deben el so baxu LUMO a una interacción favorable ente l'orbital sigma antienlazante del siliciu con un orbital pi antienlazante del fragmentu butadieno.
Siliciu hipercoordinado[editar | editar la fonte]
A diferencia del carbonu, los compuestos de siliciu pueden presentar coordinación con cinco átomos, como asocede nun grupu de compuestos que van dende los llamaos silatranos, por casu, el fenilsilatrano, a un únicu pentaorganosilicato estable:[19]
Ver tamién[editar | editar la fonte]
- Compuestos de carbonu con elementos del periodu 3: compuestu de organoaluminio, compuestu de organosilicio, compuestu de organofósforo, compuestu de organoazufre,
- Compuestos de carbonu con otros elementos del grupu 14: compuestu de organosilicio, compuestu de organogermanio, compuestu de organoestaño, compuestu de organoplomo.
Plantía:Enllaces químicos con carbonu
- sililenos, compuestos homólogos del carbeno y los sililenoides que son homólogos de los carbenoides.
Referencies[editar | editar la fonte]
- ↑ Silicon in Organic Synthesis Colvin, Y. Butterworth: London 1981
- ↑ Organosilicon Chemistry S. Pawlenko Walter de Gruyter New York 1986
- ↑ Stephen D. Kinrade, Ashley-M. Y. Gillson and Christopher T. G. Knight (2002), Silicon-29 NMR evidence of a transient hexavalent silicon complex in the diatom Navicula pelliculosa. J. Chem. Soc., Dalton Trans., 307 - 309, DOI: 10.1039/b105379p
- ↑ Handbook of Chemistry and Physics, 81st Edition CRC Press ISBN 0-8493-0481-4
- ↑ Mechanistic insight into copper-catalysed allylic substitutions with bis(triorganosilyl) zincs. Enantiospecific preparation of -chiral silanes Eric S. Schmidtmann and Martin Oestreich Chem. Commun., 2006, 3643 - 3645, doi 10.1039/b606589a
- ↑ Por aciu marcáu isotópicu puede demostrase la desimetrización sobre'l sustratu (sustituyendo átomos d'hidróxenu por átomos marcaos de deuteriu); la reacción nun dar# en traviés del compuestu entemediu π-alilo simétricu 5 que daría un amiestu a partes iguales de 3 yv3 b, sinón al traviés del entemediu Π-δ 4 que solo da como productu'l compuestu 3, al traviés d'un pasu d'adición oxidativa/eliminación reductiva.
- ↑ The Sila-Explosives Si(CH2N3)4 and Si(CH2ONO2)4: Silicon Analogues of the Common Explosives Pentaerythrityl Tetraazide, C(CH2N3)4, and Pentaerythritol Tetranitrate, C(CH2ONO2)4 Thomas M. Klapötke, Burkhard Krumm, Rainer Ilg, Dennis Troegel, and Reinhold Tacke J. Am. Chem. Soc.; 2007; ASAP Web Release Date: 04-Mayu-2007; (Artículu n'inglés) doi 10.1021/ja071299p
- ↑ Sila-Explosives Offer A Better Bang Stephen K. Ritter Chemical & Engineering News 7 de Mayu de 2007Link
- ↑ Preparation of Triethylsilicon Halides Y. A. Flood J. Am. Chem. Soc.; 1933; 55(4) pp 1735 - 1736; doi 10.1021/ja01331a504
- ↑ Radical Reduction of Aromatic Azides to Amines with Triethylsilane Luisa Benati, Giorgio Bencivenni, Rino Leardini, Matteo Minozzi, Daniele Nanni, Rosanna Scialpi, Piero Spagnolo, and Giuseppe Zanardi Elumalai Palani., ''J. Org. Chem''.; 2006; 71(15) pp 5822 - 5825; (Note) doi 10.1021/jo060824k
- ↑ From Carbon Dioxide to Methane: Homogeneous Reduction of Carbon Dioxide with Hydrosilanes Catalyzed by Zirconium-Borane Complexes Tsukasa Matsuo and Hiroyuki Kawaguchi J. Am. Chem. Soc.; 2006; 128(38) pp 12362 - 12363; doi 10.1021/ja0647250
- ↑ Effect of the synthetic method of Pt/MgO in the hydrosilylation of phenylacetylene Eulalia Ramírez-Oliva, Alejandro Hernández, J. Merced Martínez-Rosales, Alfredo Aguilar-Elguezabal, Gabriel Herrera-Pérez, and Jorge Cervantesa Arkivoc 2006 (v) 126-136 Link
- ↑ Silylenes, Silenes, and Disilenes: Novel Silicon-Based Reagents for Organic Synthesis? Henrik Ottosson and Patrick G. Steel Chem. Eur. J. 2006, 12, 1576 – 1585 doi 10.1002/chem.200500429
- ↑ The thermal decomposition of 1,1-dimethyl-1-silacyclobutane and some reactions of an unstable intermediate containing a silicon–carbon double bond L. Y. Gusel'Nikov and M. C. Flowers Chem. Commun. (London), 1967, 864 - 865, doi 10.1039/C19670000864
- ↑ A solid silaethene: isolation and characterization Adrian G. Brook, Fereydon Abdesaken, Brigitte Gutekunst, Gerhard Gutekunst and R. Krishna Kallury J. Chem. Soc., Chem. Commun., 1981, 191 - 192, doi 10.1039/C39810000191
- ↑ Química organometálica de los metales de transición. Robert H. Crabtree. Universitat Jaume I, 1997. ISBN 8480211342. Páx.184
- ↑ Direct synthesis of 2,5-dihalosiloles Organic Syntheses 2008, 85, 53-63 http://www.orgsynth.org/orgsyn/pdfs/V85P0053.pdf
- ↑ Synthesis of new dipyridylphenylaminosiloles for highly emissive organic electroluminescent devices Laurent Aubouy, Philippe Gerbier, Nolwenn Huby, Guillaume Wantz, Laurence Vignau, Lionel Hirsch and Jean-Marc Jano New J. Chem., 2004, 28, 1086 - 1090, doi 10.1039/b405238b
- ↑ Tetraalkylammonium pentaorganosilicates: the first highly stable silicates with five hydrocarbon ligands Sirik Deerenberg, Marius Schakel, Adrianus H. J. F. de Keijzer, Mirko Kranenburg, Martin Lutz, Anthony L. Spek, Koop Lammertsma, Chem. Commun., 2002, (4),348-349 doi 10.1039/b109816k
Enllaces esternos[editar | editar la fonte]
- Magnus Walter's Selected Aspects of Organosilicon Chemistry (n'inglés)
- Silicon in organic synthesis (n'inglés)
- Safety data for methyltrichlorosilane. Departamentu de Química. Universidá d'Oxford. (n'inglés)
- S. Marsden (Editor): Contemporary organosilicon chemistry. Serie temática nel Beilstein Journal of Organic Chemistry d'accesu llibre.