Carbonatu de sodiu
| Carbonatu de sodiu | |
|---|---|
 | |
| Xeneral | |
| Estructura química |
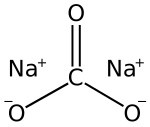 |
| Fórmula química | CNa₂O₃, Na₂CO₃ |
| SMILES canónicu | [O-)[O-].[Na+].[Na+]&zoom=2.0&annotate=none modelu 2D] |
| MolView | [O-)[O-].[Na+].[Na+] modelu 3D] |
| Propiedaes físiques | |
| Masa | 105,964 unidá de masa atómica |
| Densidá absoluta | 2,53 gramu por centímetru cúbicu |
| Puntu de fusión | 852 grau Celsius, 858,1 grau Celsius |
| Propiedaes termoquímiques | |
| Peligrosidá | |
| Identificadores | |
El carbonatu de sodiu o carbonatu sódicu ye una sal blanca y tresllúcida de fórmula química Na2CO3, usada ente otres coses na fabricación de xabón, vidriu y tintes. Ye conocíu comúnmente como barrilla, natrón, sosa Solvay, soda Solvay, sosa Ash, ceniza de soda y carbonatu sódicu anhidro[1] o a cencielles sosa,(nun s'hai de confundir cola soda cáustica, que ye un deriváu del carbonatu sódicu, por aciu un procesu conocíu como caustificación). Ye la sustancia alcalino mas común que se conoz y utiliza dende l'antigüedá.[2]
Puede topase na naturaleza o llograse artificialmente, gracies a un procesu escurrío y patentao en 1791 pol médicu y químicu francés Nicolás Leblanc. El procesu Leblanc implicaba les siguientes reacciones químiques:
- Reacción de sal común con ácidu sulfúrico: 2 NaCl + H2SO4 → Na2SO4 + 2 HCl
- Reacción de calcinación de Na2SO4 con caliar y carbón: Na2SO4 + CACU3 + 2 C → Na2CO3 + CaS + 2 CO2[2]
Más palantre esti métodu foi sustituyíu pol métodu Solvay escurríu pol químicu belga Ernest Solvay. Solvay fundó en 1863 la compañía Solvay onde utilizó profusamente el so métodu que consiguía abaratar entá más el procesu y esaniciar dalgunos de los problemes que presentaba'l métodu Leblanc. Esti métodu utiliza como materies primes el cloruru de sodiu (sal común), el amoniacu y el carbonatu de calciu (piedra caliar). En 1915 cerróse la última fábrica de sosa Leblanc.[2]
Usos[editar | editar la fonte]
El carbonatu de sodiu ye usáu pa turrar (calecer so una rabasera d'aire) el cromu y otros estractos y mengua el conteníu d'azufre y fósforu de la fundición y del aceru. Na fabricación de deterxentes, el carbonatu de sodiu ye indispensable nes formulaciones en visu a asegurar el correutu funcionamientu del restu de sustancies que lo componen, enzimes, tensioactivos, etc. mientres les distintes fases de la llavadura. Nun ye de menos importancia l'empléu del carbonatu de sodiu naquellos procesos nos qu'hai que regular el pH de distintes soluciones, referímonos al tratamientu d'agües de la industria, según nos procesos de flotación. Cerámica, xabones, llimpiadores, ablandador d'agües dures, refinamientu de petroleos, producción d'aluminiu, testiles, magaya y papel. Procesamientu metalúrxicu, preparación de productos farmacéuticos, soda cáustica por aciu el procesu de la caustificación, bicarbonatu de sodiu, nitratu de sodiu y dellos otros usos. El carbonatu de sodiu y los sos derivaos usar pa baxar el puntu de fusión del siliciu y poder trabayalo meyor, tamién apurre'l sólidu necesariu pa formar la rede.[2]
Tamién s'usa como elevador de pH para piscines: 300 gramos cada 50 m³ aumenta 0,1 puntos el valor del pH.
Ver tamién[editar | editar la fonte]
Referencies[editar | editar la fonte]
- ↑ Error de cita: La etiqueta
<ref>nun ye válida; nun se conseñó testu pa les referencies nomaesficha1 - ↑ 2,0 2,1 2,2 2,3 Los procedimientos clásicos de fabricación de la sosa. Universidá de Castiella - La Mancha. páxs. 293-309. https://previa.uclm.es/ab/educacion/ensayos/pdf/revista14/14_20.pdf. Consultáu'l 15 de febreru de 2018.
Enllaces esternos[editar | editar la fonte]
- IPCS International Programme on Chemical Safety Ficha de seguridá (n'español)

