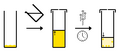
Cristalización
Esti artículu o seición necesita referencies qu'apaezan nuna publicación acreitada, como revistes especializaes, monografíes, prensa diaria o páxines d'Internet fiables. |
| Cristalización | |
|---|---|
|
Autoensamblaje (es) | |
 | |
La cristalización ye un procesu químicu pol cual a partir d'un gas, un líquidu o una disolución, los iones, átomos o molécules establecen enllaces hasta formar una rede cristalina, la unidá básica d'un cristal. La cristalización emplegar con bastante frecuencia en química para purificar una sustancia sólida.[1]
Métodu de separación de sistemes materiales homoxéneos
[editar | editar la fonte]Dexa dixebrar sustancies que formen un sistema material homoxéneu, por casu: l'agua potable ye una solución formada per agua y sales disueltos nella. La operación de cristalización ye'l procesu per mediu del cual dixébrase un componente d'una solución líquida tresfiriéndolo a la fase sólida en forma de cristales que bastien. Ye una operación necesaria pa tou productu químicu que se presenta comercialmente en forma de polvos o cristales, yá sía'l azucre o sacarosa, el sal común o cloruru de sodiu.
Enfriamientu d'una disolución concentrada
[editar | editar la fonte]Si prepara una disolución concentrada a altes temperatures y esfrezse, fórmase una disolución sobre enchida, que ye aquella que tien, momentáneamente, más soluto disueltu que l'almitible pola disolución a esa temperatura en condiciones d'equilibriu. Darréu, puede consiguise que la disolución cristalice por aciu un enfriamientu controláu. Esto realízase por que los cristales tengan un tamañu mediu, yá que si los cristales son bien pequeños les impureces queden depositaes na superficie de tola masa, y si los cristales son bien grandes les impureces queden atrapaes dientro de les redes cristalines. Esencialmente cristaliza'l compuestu principal, y les que s'arriquecen coles impureces presentes na amiestu inicial al nun algamar la so llende de solubilidá.[2]
Por que pueda emplegase esti métodu de purificación tien d'haber una variación importante de la solubilidá cola temperatura, lo que non siempres ye'l casu. El sal marino (NaCl), por casu, tien esti efeutu.
Cambéu de disolvente
[editar | editar la fonte]Preparando una disolución concentrada d'una sustancia nun bon disolvente y añadiendo un disolvente pero que ye miscible col primeru, el principal del sólidu disueltu empieza a bastiar, y enaguar madres arriquécense relativamente nes impureces. Por casu, puede dixebrase acedu benzoico d'una disolución d'ésti n'acetona amestando agua.
Evaporación del disolvente
[editar | editar la fonte]De manera análoga, evaporando el disolvente d'una disolución puede consiguise qu'empiecen a cristalizar los sólidos que taben eslleíos cuando s'algamar les llendes de les sos solubilidaes. Esti métodu foi utilizáu mientres milenios na fabricación de sal a partir de salmoria o agua marino, etc.
Sublimación
[editar | editar la fonte]En dellos compuestos la presión de vapor d'un sólidu puede aportar a lo bastante alzada como para evaporar cantidaes notables d'esti compuestu ensin algamar el so puntu de fusión (sublimación). Los vapores formaos entiesten en zones más fríes ufiertaes por casu en forma d'un "deu fríu", pasando davezu direutamente del estáu gaseosu al sólidu, (sublimación regresiva) dixebrándose, d'esta manera, de les posibles impureces. Siguiendo esti procedimientu pueden llograse sólidos puros de sustancies que subliman con facilidá como la cafeína, el azufre elemental, el acedu salicílico, el yodu, etc.
Enfriamientu selectivu d'un sólidu fundíu
[editar | editar la fonte]Pa purificar un sólidu cristalín ésti puede fundise. Del líquidu llográu cristaliza, de primeres, el sólidu puru, arriqueciéndose, la fase líquida, de les impureces presentes nel sólidu orixinal. Por casu, este ye'l métodu que s'utiliza nel llogru de siliciu ultra puru pa la fabricación de sustratos o oblees na industria de los semiconductores. Al material sólido (siliciu ensin purificar que se llogra primeramente nun horno llétricu d'inducción) dáse-y forma cilíndrica. Depués llévase a cabu una fusión per zones sobre'l cilindru. Empieza fundiéndose una franxa o seición del cilindru por un estremu y muévese dicha zona a lo llargo d'este hasta llegar al otru estremu. Como les impureces son solubles nel fundíu van dixebrándose del sólidu y abasnar escontra l'otru estremu. Esti procesu de fusión zonal puede faese delles vegaes p'asegurase que'l grau de pureza sía'l deseyáu. Finalmente, córtase l'estremu nel que s'atroparon les impureces y dixébrase del restu. La ventaya d'esti procesu ye que controlando afechiscamente la temperatura y la velocidá a la que la franxa de fundíu mover pola pieza cilíndrica, puede llograse un material que ye un monu cristal de siliciu que presenta les cares de la rede cristalina empobinaes na manera deseyada.
Crecedera cristalina
[editar | editar la fonte]
Pa llograr cristales grandes de productos pocu solubles desenvolviéronse otres téuniques. Por casu, puede faese espublizar dos compuestos de partida nuna matriz xelatinosa. Asina'l compuestu fórmase amodo dando llugar a cristales mayores. Sicasí, polo xeneral, cuanto más lentu ye'l procesu de cristalización tantu meyor suel ser la resultancia con al respective de la llimpieza de los productos de partida y tanto mayor suelen ser los cristales formaos. La forma y el tamañu de los cristales pueden ser influyíos a aparte por condicionantes como'l disolvente o la concentración de los compuestos, añadiendo traces d'otros componentes como proteínes (esta ye la manera con que los moluscos, les diatomees, los corales, etc., consiguen depositar les sos conches o cadarmes de calcita o cuarzu na forma deseyada.)
La teoría más aceptada pa esti fenómenu ye que la crecedera cristalina realízase formando capes monomoleculares alredor de xerme de cristalización o d'un cristalito inicial. Nueves molécules xúntense preferentemente na cara onde la so adhesión llibera más enerxía. Les diferencies enerxétiques suelen ser pequeñes y pueden ser modificaes pola presencia de diches impureces o camudando les condiciones de cristalización.
N'ensame d'aplicaciones puede precisase el llogru de cristales con una determinada forma y/o tamañu como: la determinación de la estructura química por aciu difracción de rayos X, la nanoteunoloxía, el llogru de películes especialmente sensibles constituyíes por cristales de sales de plata planos empobinaos perpendicularmente a la lluz d'incidencia, la preparación de los principios activos de los fármacos, etc…
Recristalización
[editar | editar la fonte]Repitir el procesu de cristalización nuna disolución que yá se fixo dichu procesu. Les agües que queden entá contienen soluto disueltu que puede cristalizase. Pa un procesu de cristalización más rápidu, aplicar un nucleu de cristalización.
Referencies
[editar | editar la fonte]- ↑ «Universidá de Burgos». Archiváu dende l'orixinal, el 2014-10-23.
- ↑ Universidá de Barcelona